题目内容
6.设NA表示阿伏加德罗常数,下列叙述正确的是( )| A. | 1molAlCl3在熔融状态时离子总数为0.4NA | |
| B. | 2.2 g分子式为 2H218O的水中含有的中子数为1.2 NA | |
| C. | 电解饱和食盐水时,当阴极产生H2 22.4L时,电路中转移的电子数为2NA | |
| D. | 常温下pH=1的H2SO4溶液中,H+的浓度为0.2mol/L |
分析 A.氯化铝为共价化合物;
B.2H218O中含有的中子数为12;
C.气体状态未知;
D.依据pH=-lg[H+]解答.
解答 解:A.氯化铝是共价化合物,熔融状态时不能电离出离子,故A错误;
B.2.2g 2H218O的物质的量为$\frac{2.2g}{22g/mol}$=0.1mol,故含有的中子数为0.1×12=1.2mol,即1.2NA,故B正确;
C.气体状态未知,气体摩尔体积不确定,无法计算氢气的物质的量,故C错误;
D.常温下pH=1的H2SO4溶液中,H+的浓度为0.1mol/L,故D错误;
故选:B.
点评 本题考查阿伏加德罗常数的有关计算和判断,明确氯化铝的性质、气体摩尔体积使用条件、pH的含义是解题关键,题目难度不大.

练习册系列答案
相关题目
16.要除去下表所列有机物中的杂质(括号内为杂质),从(1)中选择适宜的试剂,从(2)中选择分离提纯的方法,用序号填入表中.
(1)试剂:a.溴水 b.氢氧化钠溶液 c.碳酸钠溶液 d.生石灰 e.酸性高锰酸钾溶液
(2)方法:A.过滤 B.分液 C.蒸馏 D.洗气
(1)试剂:a.溴水 b.氢氧化钠溶液 c.碳酸钠溶液 d.生石灰 e.酸性高锰酸钾溶液
(2)方法:A.过滤 B.分液 C.蒸馏 D.洗气
| 要提纯的物质 (杂质) | 乙烷 (乙烯) | 乙酸乙酯 (乙酸) | 乙醇 (水) | 溴苯 (溴) |
| 选用试剂 | ||||
| 分离方法 |
17.下列反应中,反应后固体物质增重的是( )
| A. | 氢气通过灼热的CuO粉末 | B. | 二氧化碳通过Na2O2粉末 | ||
| C. | CO高温下还原Fe2O3 | D. | 将锌粒投入Cu(NO3)2溶液 |
14.下列实验操作正确的是( )
| A. | 用玻璃棒蘸取CH3COOH溶液,点在用水湿润的pH试纸上测定其pH | |
| B. | 用25ml碱式滴定管量取20.00 mL KMnO4溶液 | |
| C. | 为除去苯中的少量苯酚,向混合物中加入适量的氢氧化钠后分液 | |
| D. | 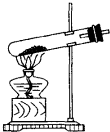 用如图装置加热分解NaHCO3 |
1.下列离子方程式书写错误的是( )
| A. | 小苏打与烧碱溶液反应:HCO3-+OH-═CO32-+H2O | |
| B. | 硫酸铜与氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ | |
| C. | 向氯化铝溶液中加入足量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 钠与水的反应 2Na+2H2O═2Na++2OH-+H2↑ |
18.在密闭容器中合成氨反应:N2(g)+3H2(g)?2NH3(g),在下列情况下,不能使反应速度加快的是( )
| A. | 加入氮气 | B. | 扩大容器体积,减小压强 | ||
| C. | 加入适量催化剂 | D. | 适当升高温度 |
16.向含1mol KAl(SO4)2的溶液中逐滴加入2mol Ba(OH)2溶液,下列说法中正确的是( )
| A. | 先生成沉淀,后沉淀全部溶解 | |
| B. | 最后的沉淀为2 mol BaSO4、1 mol Al(OH)3 | |
| C. | 当溶液中SO42-全部沉淀出来时,沉淀的总质量最大 | |
| D. | 当溶液中Al3+全部沉淀出来时,沉淀的总质量最大 |
 (1)写出由甲苯制备TNT的化学反应方程式
(1)写出由甲苯制备TNT的化学反应方程式 ;
; .
. ;Y的结构简式为:
;Y的结构简式为: .
.