题目内容
在标准状况下,①4g H2、②11.2L O2、③1mol H2O中,含原子数最多的是 ,体积最小的是 .(填序号)
考点:物质的量的相关计算
专题:
分析:根据n=
=
计算氢气、氧气物质的量,氢气含有原子物质的量为氢气的2倍,氧气含有原子物质的量为氧气的2倍,水含有原子物质的量为水的3倍,物质的量越大含有原子数目越多,根据V=nVm计算氢气体积,标况下水为液态,根据m=nM计算水的质量,密度约是1g/mL,根据V=
计算水的体积.
| m |
| M |
| V |
| Vm |
| m |
| ρ |
解答:
解:4g氢气的物质的量为
=2mol,含有原子物质的量为2mol×2=4mol,体积为2mol×22.4L/mol=44.8L;
标况下,11.2L氧气物质的量为
=0.5mol,含有原子物质的量为0.5mol×3=1.5mol,
1mol H2O中含有原子物质的量为0.5mol×2=1mol,质量为18g,体积约是
=18mL,
故含原子数最多的是①4g H2,体积最小的是③1mol H2O,
故答案为:①;③.
| 4g |
| 2g/mol |
标况下,11.2L氧气物质的量为
| 11.2L |
| 22.4L/mol |
1mol H2O中含有原子物质的量为0.5mol×2=1mol,质量为18g,体积约是
| 18g |
| 1g/mL |
故含原子数最多的是①4g H2,体积最小的是③1mol H2O,
故答案为:①;③.
点评:本题考查物质的量有关计算,难度不大,注意对公式的理解,有利于基础知识的巩固.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
下列热化学方程式中的△H能表示可燃物的燃烧热的是( )
| A、2H2S(g)+O2(g)=2S (s)+2H2O(l)△H=-Q2 kJ/mol | ||
| B、CH4(g)+2O2(g)═CO2(g)+2H2O(g);△H=-802.3kJ/mol | ||
C、CO(g)+
| ||
| D、2H2(g)+O2(g)═2H2O(1);△H=-571.6kJ/mol |
下列说法正确的是( )
| A、常温下,反应2A (s)+B (g)=2C (g)+D (g)不能自发进行,则该反应△H一定大于0 |
| B、铜的金属活动性比铁弱,可在海轮外壳上装若干铜块以减缓船体的腐蚀速率 |
| C、其他条件不变,向纯水中加入盐酸或氢氧化钠都能抑制水的电离,降低水的离子积 |
| D、能与酸反应的氧化物,一定是碱性氧化物 |
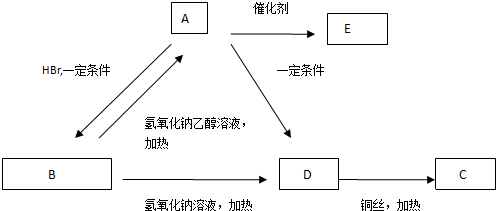
 )是一种天然抗癌药物,在一定条件下发生如下转化:
)是一种天然抗癌药物,在一定条件下发生如下转化: