题目内容
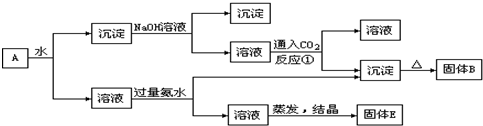
某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3在一定条件下可实现下图所示的物质之间的变化:
据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是________________________。
(2)根据上述框图反应关系,写出下列B、C、D、E所含物质的化学式:
固体B_______________;沉淀C_______________;
沉淀D_______________;溶液E_______________。
(3)写出①②③④四个反应的离子方程式:
①__________________________________________________________________;
②__________________________________________________________________;
③__________________________________________________________________;
④__________________________________________________________________。
解析:KAl(SO4)2、Al2O3和Fe2O3溶于水,KAl(SO4)2溶于水,Al2O3和Fe2O3不溶于水,所以沉淀C为Al2O3和Fe2O3;Al2O3溶于碱,生成偏铝酸钠, Fe2O3不溶于碱,所以D为Fe2O3,偏铝酸钠与适量盐酸反应生成氢氧化铝沉淀,加热分解生成氧化铝。KAl(SO4)2与氨水反应生成硫酸钾、硫酸铵和氢氧化铝沉淀,即E为K2SO4和(NH4)2SO4。
答案:(1)过滤
(2)Al2O3 Al2O3和Fe2O3 Fe2O3 K2SO4和(NH4)2SO4
(3)①Al2O3+2OH-+3H2O![]() 2[Al(OH)4]-
2[Al(OH)4]-
②Al3++3NH3·H2O![]() Al(OH)3↓+
Al(OH)3↓+![]()
③[Al(OH)4]-+H+![]() Al(OH)3↓+H2O
Al(OH)3↓+H2O
④2Al(OH)3![]() Al2O3+3H2O
Al2O3+3H2O