题目内容
3.在标准状况下.有1L的甲烷和氢气混合气.试求在下列情况下,甲烷和氢气的质量各是多少?(1)它们的体积相同;
(2)它们的物质的量相同;
(3)它们的质量相同;
(4)它们所含的原子相同;
(5)它们所含的电子数相同.
分析 根据n=$\frac{V}{Vm}$=$\frac{m}{M}$,结合分子和原子的组成分析解答.
解答 解:在标准状况下.有1L的甲烷和氢气混合气;
(1)它们的体积相同,则甲烷和氢气均为0.5L,则n=$\frac{0.5L}{22.4L/mol}$=$\frac{0.5}{22.4}$mol,
m(甲烷)=$\frac{0.5}{22.4}$mol×16g/mol=0.357g;m(氢气)=$\frac{0.5}{22.4}$mol×2g/mol=0.0446g;
答:甲烷和氢气的质量分别为0.357g、0.0446g;
(2)它们的物质的量相同,则体积相同,所以n=$\frac{0.5L}{22.4L/mol}$=$\frac{0.5}{22.4}$mol,
m(甲烷)=$\frac{0.5}{22.4}$mol×16g/mol=0.357g;m(氢气)=$\frac{0.5}{22.4}$mol×2g/mol=0.0446g;
答:甲烷和氢气的质量分别为0.357g、0.0446g;
(3)设甲烷和氢气的质量为xg,
则$\frac{xg}{16g/mol}$×22.4L/mol+$\frac{xg}{2g/mol}$×22.4L/mol=1L,解得x=0.079g;
答:甲烷和氢气的质量分别为0.079g、0.079g;
(4)设甲烷的物质的量为xmol,氢气的物质的量为ymol;
则(x+y)×22.4=1L,5x=2y,解得x=$\frac{1}{78.4}$mol,y=$\frac{5}{78.4}$mol,
所以m(甲烷)=$\frac{1}{78.4}$mol×16g/mol=0.204g;m(氢气)=$\frac{5}{78.4}$mol×2g/mol=0.128g;
答:甲烷和氢气的质量分别为0.204g、0.128g;
(5)设甲烷的物质的量为xmol,氢气的物质的量为ymol;
则(x+y)×22.4=1L,10x=2y,解得x=$\frac{1}{134.4}$mol,y=$\frac{5}{134.4}$mol,
所以m(甲烷)=$\frac{1}{134.4}$mol×16g/mol=0.119g;m(氢气)=$\frac{5}{134.4}$mol×2g/mol=0.0744g;
答:甲烷和氢气的质量分别为0.119g、0.0744g.
点评 本题考查了有关混合物的计算,题目难度中等,注意掌握物质的量与摩尔质量、气体摩尔体积之间的转化关系,明确有关混合物计算的方法,试题有利于培养学生的分析、理解能力及化学计算能力.

 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案①纯碱溶液去油污;②铁在潮湿的环境下生锈;③NH4Cl与ZnCl2溶液可作焊接中的除锈剂;④盛放Na2CO3溶液的试剂瓶应用橡皮塞,而不用玻璃塞;⑤酸雨在空气中放置一段时间pH降低;⑥草木灰与铵态氮肥不能混合施用( )
| A. | ①③④⑥ | B. | ①②⑤⑥ | C. | ①③④⑤ | D. | 全有关 |
| A. | 随着电解的进行,溶液的pH减小 | |
| B. | OH-向阳极移动,阳极附近溶液呈碱性 | |
| C. | 阴极上H+得电子被还原成H2 | |
| D. | NO3-向阳极移动,K+向阴极移动,分别在对应的电极上析出 |
| A. | FeCl2溶液(KSCN) | B. | KOH(盐酸) | ||
| C. | Na2SO3溶液(BaCl2) | D. | HCHO溶液(石蕊试液) |

将收集的三瓶CO2置于天平上称量,若三个集气瓶的体积与质量均相等,称量结果正确的是( )
| A. | ①最重 | B. | ②最重 | C. | ③最重 | D. | ①②③一样重 |
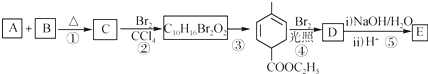
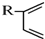 +
+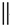 $\stackrel{△}{→}$
$\stackrel{△}{→}$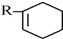
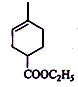 +Br2→
+Br2→ .
.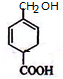 .
.
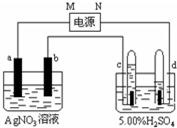 如图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极.试管充满水,通电一段时间后,在c、d两极上共收集到标准状态下336mL气体,体积如图所示.请回答下列问题.
如图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极.试管充满水,通电一段时间后,在c、d两极上共收集到标准状态下336mL气体,体积如图所示.请回答下列问题.