题目内容
17.下列物质①Al2O3 ②Al(OH)3 ③NaHSO4 ④NaHCO3⑤Mg(OH)2 ⑥NaClO中,既能与强酸反应又能与强碱反应的是( )| A. | ①②④ | B. | ②③④⑥ | C. | ①②④⑤ | D. | ①②③④⑤⑥ |
分析 Al、两性氧化物、两性氢氧化物、弱酸酸式盐、弱酸的铵盐、蛋白质、氨基酸等物质都能和强酸、强碱反应,据此分析解答.
解答 解:①Al2O3属于两性氧化物,能和强酸、强碱反应生成盐和水,故正确;
②Al(OH)3属于两性氢氧化物,能和强酸、强碱反应生成盐和水,故正确;
③NaHSO4属于强酸酸式盐,能和强碱反应但不能和强酸反应,故错误;
④NaHCO3属于强碱弱酸酸式盐,能和强酸、强碱反应,故正确;
⑤Mg(OH)2属于碱,能和强酸反应但不能和强碱反应,故错误;
⑥NaClO属于弱酸强碱盐,能和强酸反应但不能和强碱反应,故错误;
故选A.
点评 本题考查元素化合物,为高频考点,明确元素化合物性质及物质之间的转化是解本题关键,熟练掌握常见元素化合物性质并灵活运用,知道铝及其化合物的特殊性,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列物质在氧气中燃烧只生成CO2和H2O的是( )
| A. | 烷烃 | B. | 卤代烃 | C. | 蛋白质 | D. | 橡胶 |
5.向某密闭容器中充入1mol CO和2mol H2O(g),发生反应:CO+H2O(g) $?_{高温}^{催化剂}$CO2+H2,当反应达到平衡时,CO的体积分数为x,若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是( )
| A. | 0.5 mol CO+2 mol H2O(g)+1 mol CO2+1 mol H2 | |
| B. | 1 mol CO+1 mol H2O(g)+1 mol CO2+1 mol H2 | |
| C. | 0.5 mol CO+1.5 mol H2O(g)+0.4 mol CO2+0.4 mol H2 | |
| D. | 0.5 mol CO+1.5 mol H2O(g)+0.5 mol CO2+0.5 mol H2 |
2.下列叙述不正确的是( )
| A. | 有化学键被破坏的变化不一定是化学变化 | |
| B. | 金属元素与非金属元素原子间形成的化学键不一定是离子键 | |
| C. | 乙炔分子中,σ键与π键数目之比为1:1 | |
| D. | 金刚石中碳原子采取sp3杂化,12g金刚石中含2mol 碳碳单键 |
9.标准状况下有三种气体:①6.72L NH3 ②1.204×1023个 H2S ③5.6g CH4,下列关系正确的是( )
| A. | 体积大小:③>②>① | B. | 原子数目:③>①>② | C. | 密度大小:②>③>① | D. | 质量大小:②>③>① |
6.碱金属具有特征的性质是( )
| A. | 具有银白色金属光泽 | B. | 良好的导热性 | ||
| C. | 较强的还原性 | D. | 优良的导电性 |
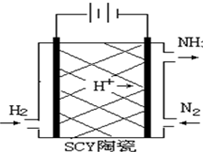 科学家采用质子高导电性的SCY陶瓷(可传递H+)实现了低温常压下高转化率的电化学合成氨,其实验原理示意图如图所示,则阴极的电极反应式是反应式为N2+6H++6e-=2NH3.
科学家采用质子高导电性的SCY陶瓷(可传递H+)实现了低温常压下高转化率的电化学合成氨,其实验原理示意图如图所示,则阴极的电极反应式是反应式为N2+6H++6e-=2NH3.