题目内容
13.下列有关颜色变化的叙述不正确的是( )| A. | 淀粉溶液中滴入碘水--变蓝色 | B. | KSCN溶液中滴入Fe3+--变血红色 | ||
| C. | 氯化银见光分解--变银白色 | D. | 无水硫酸铜在空气中久置--变蓝色 |
分析 A.碘单质遇淀粉变蓝是碘单质的特征性质;
B.根据三价铁遇硫氰化钾溶液变成血红色;
C.氯化银分解生成单质银;
D.无水硫酸铜能够与水蒸气结合生成胆矾.
解答 解:A.淀粉溶液遇单质碘显蓝色是碘单质的特征性质,可用于碘单质的检验,故A正确;
B.三价铁遇硫氰化钾溶液变成血红色,所以氯化铁溶液中滴加硫氰化钾溶液变成血红色,故B正确;
C.氯化银分解生成单质银,为黑色粉末,故C错误;
D.无水硫酸铜能够与水蒸气结合生成胆矾,胆矾为蓝色,故D正确;
故选C.
点评 本题考查了物质的性质应用,通过颜色的变化考查物质的性质,题目难度不大,注意银粉和晶体银的颜色区别.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
3.下列物质中均含杂质(括号中是杂质),除杂质方错误的是( )
| A. | 碳酸钠(碳酸氢钠):加热,直到质量不再减少为止 | |
| B. | 溴苯(溴):加入氢氧化钠溶液洗涤,分液 | |
| C. | 乙醇(乙醛):加入新制氢氧化铜煮沸,过滤 | |
| D. | 乙酸丁酯(乙酸):加入碳酸钠溶液洗涤,分液 |
4.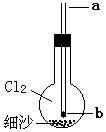 如图烧瓶内充满氯气,底部有层细沙(不参与反应),b处塞有小块钠.从a口用细铁丝把钠送下去,再从a口滴下一滴水,恰好滴在钠块上,立即剧烈反应,烧瓶内产生大量白色烟雾.不正确的说法是( )
如图烧瓶内充满氯气,底部有层细沙(不参与反应),b处塞有小块钠.从a口用细铁丝把钠送下去,再从a口滴下一滴水,恰好滴在钠块上,立即剧烈反应,烧瓶内产生大量白色烟雾.不正确的说法是( )
 如图烧瓶内充满氯气,底部有层细沙(不参与反应),b处塞有小块钠.从a口用细铁丝把钠送下去,再从a口滴下一滴水,恰好滴在钠块上,立即剧烈反应,烧瓶内产生大量白色烟雾.不正确的说法是( )
如图烧瓶内充满氯气,底部有层细沙(不参与反应),b处塞有小块钠.从a口用细铁丝把钠送下去,再从a口滴下一滴水,恰好滴在钠块上,立即剧烈反应,烧瓶内产生大量白色烟雾.不正确的说法是( )| A. | 水可能参与二个氧化还原反应 | |
| B. | Cl2可能参与四个氧化还原反应 | |
| C. | 氧元素参与的反应一定是氧化还原反应 | |
| D. | 氢元素参与的反应包含被氧化与被还原过程 |
1.用饱和氯化钠溶液润湿的滤纸分别做甲、乙两个实验,下列判断错误的是( )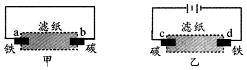

| A. | 甲是原电池,乙是电解池 | |
| B. | 甲中铁棒比乙中铁棒更易腐蚀 | |
| C. | d电极上的电极反应是:Fe-2e→Fe2+ | |
| D. | b电极上的电极反应是:O2+2H2O+4e→4OH- |
8.有关氧元素及含氧物质表示正确的是( )
| A. | 质子数为8、中子数为10的氧原子:${\;}_{8}^{18}$O | |
| B. | 氧离子(O2-)的结构示意图: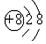 | |
| C. | 氧原子最外层p亚层电子排布式:2s22p4 | |
| D. | 某碳氧化合物电子式: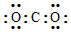 |
18.检验苯甲醛中是否含有苯甲醇可用的试剂是( )
| A. | 金属钠 | B. | 银氨溶液 | C. | 新制氢氧化铜 | D. | 饱和食盐水 |
5.下列关于实验操作说法正确的是( )
| A. | 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 | |
| B. | 中和滴定实验中,锥形瓶用蒸馏水洗净须经烤箱烘干后才可使用 | |
| C. | 配制0.5mol•L-1、480mL的NaOH溶液需称量9.6g的NaOH固体作溶质 | |
| D. | 某溶液中滴入2滴K3[Fe(CN)6]溶液生成具有特征蓝色的沉淀,说明原溶液中含有Fe2+ |
2.用下列装置完成相关实验,合理的是( ) )
| A. | 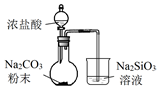 验证H2CO3酸性强于H2SiO3 | B. | 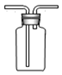 收集CO2或NH3 | ||
| C. | 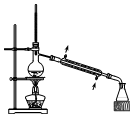 分离Na2CO3溶液与CH3COOC2H5 | D. | 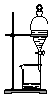 分离CH3CH2OH与CH3COOC2H5 |
2.下列有关说法正确的是( )
| A. | 氮氧化合物、PM 2.5颗粒、CO2都会导致酸雨 | |
| B. | 氯水和二氧化硫混合使用能增强漂白效果 | |
| C. | 硫酸铜溶液可用于泳池消毒是利用了Cu2+能使蛋白质盐析 | |
| D. | 轮船上挂锌锭防止铁腐蚀属于牺牲阳极的阴极保护法 |