题目内容
为了证明长期放置的硫酸亚铁溶液已经变质,可取少量溶液,加入少量 溶液.反应的离子方程式 .防止硫酸亚铁溶液变质的方法是 .相关的离子方程式: .
考点:铁盐和亚铁盐的相互转变
专题:元素及其化合物
分析:硫酸亚铁溶液易被氧化为硫酸铁,可以用硫氰化钾检验铁离子,金属铁可以和铁离子之间反应生成亚铁离子,据此回答.
解答:
解:长期放置的硫酸亚铁溶液已经变质,则其中会含有硫酸铁,可以加入硫氰化钾根据溶液是否变为血红色来检验铁离子的存在,发生反应的原理是Fe3++3SCN-=Fe(SCN)3,金属铁可以和铁离子之间反应生成亚铁离子,Fe+2Fe3+=3Fe2+,所以加入金属铁可以防止硫酸亚铁溶液变质,
故答案为:硫氰化钾;Fe3++3SCN-=Fe(SCN)3;加入铁粉;Fe+2Fe3+=3Fe2+.
故答案为:硫氰化钾;Fe3++3SCN-=Fe(SCN)3;加入铁粉;Fe+2Fe3+=3Fe2+.
点评:本题考查学生亚铁盐和铁盐的性质以及离子的检验知识,注意知识的归纳和梳理是解题的关键,难度中等.

练习册系列答案
相关题目
下列物质不是配合物的是( )
| A、NH4Cl |
| B、KAl(SO4)2?12H2O |
| C、CuSO4?5H2O |
| D、[Ag(NH3)2]OH |
短周期元素W、X、Y、Z的原子序数依次增大,W与Y原子的最外层电子数之和为X原子的最外层电子数的2倍,Z原子的最外层电子数等于其最内层电子数,X、Y、Z的简单离子的电子层结构相同,W的单质是空气中体积分数最大的气体.下列说法正确的是( )
| A、元素Y的气态氢化物比W的稳定 |
| B、元素Y的最高正价与负价绝对值的和等于8 |
| C、化合物XY2与ZY2分子中的化学键类型相同 |
| D、原子半径的大小顺序:r(W)>r(X)>r(Y)>r(Z) |
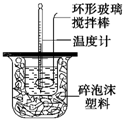 在量热器中将50ml、0.50mol?L-1CH3COOH溶液与50ml、0.55mol?L-1NaOH溶液混合,温度从25.16℃升高到27.46℃.已知量热计的热容常数(量热计各部件每升高10C所需的热量)是150J?0C-1,C=4.18J?g-1?0C-1,溶液的密度为1g?cm-3.
在量热器中将50ml、0.50mol?L-1CH3COOH溶液与50ml、0.55mol?L-1NaOH溶液混合,温度从25.16℃升高到27.46℃.已知量热计的热容常数(量热计各部件每升高10C所需的热量)是150J?0C-1,C=4.18J?g-1?0C-1,溶液的密度为1g?cm-3.
 液,试画出原电池的装置图,并说明其工作原理.
液,试画出原电池的装置图,并说明其工作原理.