题目内容
3.在下列条件下,一定能大量共存的离子组是( )| A. | 1.0mol/L的KNO3溶液:Na+、Fe2+、Cl-、SO42- | |
| B. | 含有NaOH的溶液:K+、Ba2+、HCO3-、Cl- | |
| C. | 能与Al反应生成H2的溶液:NH4+、K+、NO3-、Cl- | |
| D. | 饱和氯水中:K+、Na+、Cl-、HSO3- |
分析 A.该组离子之间不反应;
B.离子之间结合生成沉淀;
C.能与Al反应生成H2的溶液,为非氧化性酸或强碱溶液;
D.氯水中含强氧化性物质氯气、HClO等.
解答 解:A.该组离子之间不反应,可大量共存,故A正确;
B.Ba2+、HCO3-、OH-结合生成沉淀,不能共存,故B错误;
C.能与Al反应生成H2的溶液,为非氧化性酸或强碱溶液,碱溶液中不能大量存在NH4+,酸溶液中H+、NO3-、Al发生氧化还原反应不生成氢气,故C错误;
D.氯水中含强氧化性物质氯气、HClO等,与HSO3-发生氧化还原反应不能共存,故D错误;
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应、氧化还原反应的判断,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.油漆工业的原料之一Fe2O3可由FeSO4加热分解制得,请写出该反应的化学方程式2FeSO4$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+SO2↑+SO3↑..
18.下列化学用语中正确的是( )
| A. | ${\;}_{8}^{18}$O2-离子结构示意图: | B. | HClO的结构式:H-O-Cl | ||
| C. | NF3的比例模型: | D. | H2O2的电子式: |
8.铁、铜单质及其化合物应用范围很广.现有含氯化亚铁杂质的氯化铜晶体(CuCl2•2H2O),为制取纯净的CuCl2•2H2O,首先将其制成酸性水溶液,然后按如图步骤进行提纯:
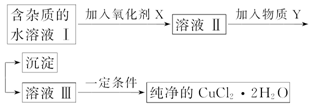
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见表:
请回答下列问题:
(1)加入氧化剂的目的是将Fe2+氧化为Fe3+,Fe3+便于生成沉淀与Cu2+分离.
(2)最适合作氧化剂X的是C,写出该反应的离子方程式:2Fe2++H2O2+2H+=2Fe3++2H2O
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(3)加入的物质Y可以是C.A.NaOH溶液 B.氨水 C.CuO D.Cu
(4)最后能不能直接蒸发结晶得到CuCl2•2H2O晶体?不能(填“能”或“不能”).若能,不用回答;若不能,回答该如何操作?应在HCl氛围中加热蒸发.

已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见表:
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 9.0 | 6.7 |
(1)加入氧化剂的目的是将Fe2+氧化为Fe3+,Fe3+便于生成沉淀与Cu2+分离.
(2)最适合作氧化剂X的是C,写出该反应的离子方程式:2Fe2++H2O2+2H+=2Fe3++2H2O
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(3)加入的物质Y可以是C.A.NaOH溶液 B.氨水 C.CuO D.Cu
(4)最后能不能直接蒸发结晶得到CuCl2•2H2O晶体?不能(填“能”或“不能”).若能,不用回答;若不能,回答该如何操作?应在HCl氛围中加热蒸发.
15.下列说法正确的是( )
| A. | 摩尔是国际七个基本物理量之一 | |
| B. | 含NA个O原子的O2物质的量为0.5mol | |
| C. | 6.02×1023个任何物质的量均为1mol | |
| D. | 1mol氢含有6.02×1023个氢 |
 .
.