题目内容
用NA表示阿伏加德罗常数的值,下列说法错误的是( )
| A、24g Mg变为Mg2+时失去的电子数为2NA |
| B、常温常压下,11.2LN2中含有的分子数为0.5NA |
| C、1L 0.1mol/LNaNO3溶液中含有的钠离子数为0.1NA |
| D、32g O2中含有氧原子的个数为2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.镁为2价金属,1mol镁完全反应失去2mol电子;
B.常温常压下,不是标准状况下,不能使用标况下的气体摩尔体积计算氮气的物质的量;
C.根据n=cV计算出硝酸钠的物质的量,再计算出钠离子的物质的量及数目;
D.氧气为双原子分子,32g氧气的物质的量为1mol,含有2mol氧原子.
B.常温常压下,不是标准状况下,不能使用标况下的气体摩尔体积计算氮气的物质的量;
C.根据n=cV计算出硝酸钠的物质的量,再计算出钠离子的物质的量及数目;
D.氧气为双原子分子,32g氧气的物质的量为1mol,含有2mol氧原子.
解答:
解:A.24g镁的物质的量为1mol,1mol镁完全反应失去2mol电子,失去的电子数为2NA,故A正确;
B.不是标况下,不能使用标况下的气体摩尔体积计算11.2L氮气的物质的量,故B错误;
C.1L 0.1mol/LNaNO3溶液中含有0.1mol硝酸钠,含有0.1mol钠离子,含有的钠离子数为0.1NA,故C正确;
D.32g氧气的物质的量为1mol,1mol氧气中含有2mol氧原子,含有氧原子的个数为2NA,故D正确;
故选B.
B.不是标况下,不能使用标况下的气体摩尔体积计算11.2L氮气的物质的量,故B错误;
C.1L 0.1mol/LNaNO3溶液中含有0.1mol硝酸钠,含有0.1mol钠离子,含有的钠离子数为0.1NA,故C正确;
D.32g氧气的物质的量为1mol,1mol氧气中含有2mol氧原子,含有氧原子的个数为2NA,故D正确;
故选B.
点评:本题考查阿伏加德罗常数的应用,题目难度中等,明确标况下气体摩尔体积的使用条件,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列说法正确的是( )
| A、用金属活动性顺序可解释反应:Na(l)+KCl(l)═NaCl(l)+K(g) |
| B、用玻璃棒蘸取某溶液滴在pH试纸上,可测得的溶液pH=2.9 |
| C、在100 mL容量瓶中溶解4.0 g NaOH,可得到1.0 mol/L的NaOH溶液 |
| D、由水的离子积常数Kw随温度升高而增大的事实,可判断水电离是吸热过程 |
在100mL含等物质的量HBr和H2SO3的溶液里通入0.01mol Cl2,有一半Br-变为Br2(已知Br2能氧化H2SO3).原溶液中HBr和H2SO3的浓度都等于( )
| A、0.0075 mol?L-1 |
| B、0.0018 mol?L-1 |
| C、0.075 mol?L-1 |
| D、0.08 mol?L-1 |
下列说法中合理的是( )
| A、味精的主要成分为蛋白质,烧菜时可加入适量 |
| B、养鸭厂添加苏丹红制“红心鸭蛋”,可使鸭蛋色泽鲜艳、美观 |
| C、汽水中添加林丹、毒死蜱和七氯苯等药剂制“××可乐”,以增强口感和余味 |
| D、将废弃塑料热裂解处理,可以获得乙烯、丙烯等化工原料 |
下列反应不属于氧化还原反应的是( )
A、2KClO3
| ||||
| B、NO+NO2+2NaOH═2NaNO2+H2O | ||||
| C、BrCl+H2O═HCl+HBrO | ||||
| D、2FeCl2+Cl2═2FeCl3 |
下列现象与氢键有关的是( )
①HF的沸点比同主族其他元素的氢化物高
②甲硫醇(CH3SH)比甲醇的沸点低
③HBr在水中的溶解性很大
④邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低
⑤H2O是一种非常稳定的化合物.
①HF的沸点比同主族其他元素的氢化物高
②甲硫醇(CH3SH)比甲醇的沸点低
③HBr在水中的溶解性很大
④邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低
⑤H2O是一种非常稳定的化合物.
| A、全部 | B、①②④ |
| C、①④⑤ | D、①②③④ |
通过复习总结,你认为下列对化学知识概括合理的是( )
| A、氧化物不可能是还原产物,只可能是氧化产物 |
| B、一种元素可能有多种氧化物,但同种化合价只对应一种氧化物 |
| C、有单质参加或有单质生成的反应一定是氧化还原反应 |
| D、碱性氧化物一定是金属氧化物 |
 表示的分子式
表示的分子式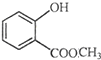 中含有的官能团的名称为
中含有的官能团的名称为