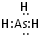题目内容
在元素周期表前四周期中,有A、B、C、D四种元素,它们的原子序数依次增大,A原子有3个未成对电子;B原子次外层有8个电子,1 mol B单质与足量盐酸反应可生成 l mol H2,B单质不易与冷水反应;C元素的+3价离子的d 轨道是半充满的;D元素易形成-1价离子。
(1)填写下表
(1)填写下表

(2)C元素位于第___周期___族,在含C2+的水溶液中,滴入氯水后再滴人数滴KSCN溶液,现象是_____________________。上述反应的离子方程式为______________。在含C3+的水溶液中加足量铁粉充分振荡 后,滴入KSCN溶液,现象是______________,上述反应的离子方程式为_______________。
(3)四种元素中电负性最大的元素是____,第一电离能最小的元素是___。A、B两种元素的原子半径大小是_______单核离子的离子半径大小是_________
(3)四种元素中电负性最大的元素是____,第一电离能最小的元素是___。A、B两种元素的原子半径大小是_______单核离子的离子半径大小是_________
(1)氮、N、1s22s22p3、p;铁、Fe、[Ar]3d64s2、d
(2)四;第Ⅷ;溶液变血红色;2Fe2++Cl2=2Fe3++2Cl-、Fe3++3SCN-=Fe(SCN)3;无明显现象;
Fe+2Fe3+=3Fe2+
(3)N;Mg;Mg>N;N3->Mg2+
(2)四;第Ⅷ;溶液变血红色;2Fe2++Cl2=2Fe3++2Cl-、Fe3++3SCN-=Fe(SCN)3;无明显现象;
Fe+2Fe3+=3Fe2+
(3)N;Mg;Mg>N;N3->Mg2+

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
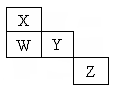 如图为元素周期表前四周期的一部分,W、X、Y、Z是元素周期表中前四周期元素,它们在周期表中的相对位置如表中所示.下列有关叙述中正确的是( )
如图为元素周期表前四周期的一部分,W、X、Y、Z是元素周期表中前四周期元素,它们在周期表中的相对位置如表中所示.下列有关叙述中正确的是( )| A、Z元素一定是金属元素 | B、X、Y、W一定是主族元素 | C、W的氢化物的沸点一定比X的氢化物的沸点高 | D、Z既可能在三周期,也可能在四周期 |
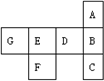 (2010?卢湾区二模)“椅子形状”的图包含了元素周期表前四周期的部分元素,其中A、B、C、D四种元素原子序数之和为77.
(2010?卢湾区二模)“椅子形状”的图包含了元素周期表前四周期的部分元素,其中A、B、C、D四种元素原子序数之和为77.