题目内容
1.标准状况下,11.2L氧气的质量是( )| A. | 8g | B. | 16g | C. | 32g | D. | 4g |
分析 根据n=$\frac{V}{{V}_{m}}$,计算标准状况下11.2L O2的物质的量,然后结合m=nM来计算求解.
解答 解:标准状况下11.2L O2的物质的量为$\frac{11.2L}{22.4L/mol}$=0.5mol,所以m=nM=0.5mol×32g/mol=16g,故选B.
点评 本题考查物质的量有关计算,比较基础,注意对公式的理解与灵活应用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.含有3.01×1023个氧原子的H2SO4的物质的量是( )
| A. | 0.500 mol | B. | 1.00 mol | C. | 0.125mol | D. | 0.25 mol |
6.下列说法正确的是( )
| A. | 纯水的pH值一定等于7 | |
| B. | [H+]大于10-7mol/L的溶液一定是酸性溶液 | |
| C. | pH=2的溶液中[H+]是pH=1的溶液的两倍 | |
| D. | [H+]=2×10-7mol/L的溶液可能是中性溶液 |
13.具有显著抗癌活性的10-羟基喜树碱的结构如图所示.下列关于10-羟基喜树碱的说法不正确的是( )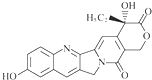

| A. | 可以与溴水反应 | |
| B. | 可以与FeCl3溶液发生显色反应 | |
| C. | 可以与浓HBr溶液反应 | |
| D. | 一定条件下,1 mol该物质最多可与1 mol NaOH反应 |
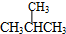 和
和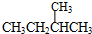 ;
;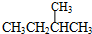 和
和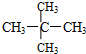 ;
;