题目内容
实验室需用2mol?L-1硫酸铜溶液450mL,配制时应选用称取硫酸铜的质量是( )
| A、144.0gCuSO4 |
| B、144.0gCuSO4?5H2O |
| C、225.0gCuSO4?5H2O |
| D、250.0gCuSO4?5H2O |
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:配制450mL的硫酸铜溶液,实验室中没有450mL的容量瓶,配制时需要选用500mL容量瓶,实际上配制的是500mL 2mol/L的硫酸铜溶液,根据n=cV计算出硫酸铜的物质的量,再根据m=nM计算出溶质硫酸铜的质量.
解答:
解:实验室需用2mol?L-1硫酸铜溶液450mL,由于没有规格为450mL的容量瓶,配制时应该选用500mL的容量瓶,
实际上配制的溶液为500mL 2mol/L的硫酸铜溶液,
则需要硫酸铜的物质的量为:n(CuSO4)=2mol/L×0.5L=1mol,
需要无水硫酸铜的质量为:m(CuSO4)=160g/mol×1mol=160g,
需要CuSO4?5H2O的质量为:m(CuSO4?5H2O)=250g/mol×1mol=250g,
故选D.
实际上配制的溶液为500mL 2mol/L的硫酸铜溶液,
则需要硫酸铜的物质的量为:n(CuSO4)=2mol/L×0.5L=1mol,
需要无水硫酸铜的质量为:m(CuSO4)=160g/mol×1mol=160g,
需要CuSO4?5H2O的质量为:m(CuSO4?5H2O)=250g/mol×1mol=250g,
故选D.
点评:本题考查了配制一定物质的量浓度的溶液中容量瓶的选用、物质的量浓度的相关计算,题目难度不大,注意掌握配制一定物质的量浓度的溶液的方法,明确物质的量浓度的相关计算方法,正确判断容量瓶规格为解答关键.

练习册系列答案
相关题目
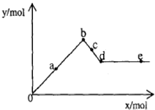 已知Ba(AlO2)2可溶于水.如图表示的是向A12(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加人Ba(OH)2的物质的量x的关系.
已知Ba(AlO2)2可溶于水.如图表示的是向A12(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加人Ba(OH)2的物质的量x的关系.说明:AlO2-即[Al(OH)4]-下列有关叙述正确的是( )
| A、a-b时沉淀的物质的量:A1(OH)3比BaSO4多 |
| B、c-d时溶液中离子的物质的量:AlO2-比Ba2+多 |
| C、a-d时沉淀的物质的量:BaSO4可能小于A1(OH)3 |
| D、d-e时溶液中离子的物质的量:整个阶段Ba2+一定不会等于OH- |
下列有关性质的比较中,大小顺序排列错误的是( )
| A、物质的熔点:石英>食盐>碘 |
| B、热稳定性:CH4>H2S>HCl>NH3 |
| C、下列元素的最高价氧化物的水化物酸碱性强弱:碱性:NaOH>Al(OH)3 酸性HClO4>H2SO4 |
| D、分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
我国“嫦娥”探月工程已正式启动.据科学家预测,月球的土壤中吸附着数百万吨的
He,每百吨
He核聚变所释放出的能量相当于目前人类一年消耗的能量.在地球上,氦元素主要以
He的形式存在.下列说法正确的是( )
3 2 |
3 2 |
4 2 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
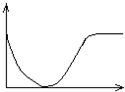 下列实验过程中产生的现象与右边坐标图形相符合的是( )
下列实验过程中产生的现象与右边坐标图形相符合的是( )