��Ŀ����
����Ŀ�����й��ڸ�ͼ��Ľ��ͻ�ó�������ȷ���ǣ� �� 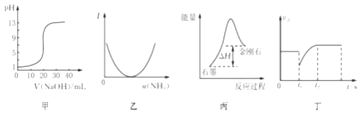
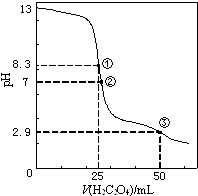
A.ͼ�ױ�ʾ0.10molL��1NaOH��Һ�ζ�20.00 mL 0.10 molL��1������Һ�ĵζ�����
B.ͼ�ұ�ʾ��������Һ��ͨ�백����������������Һ������I�ı仯
C.����ͼ����ʾ��֪��ʯīת��Ϊ���ʯ����������ʯī�Ƚ��ʯ�ȶ�
D.ͼ����ʾ��Ӧ2SO2+O22SO3 �� t1ʱ��ֻ��С�� SO3��Ũ��
���𰸡�C
���������⣺A������Ϊ���ᣬ0.10 molL��1���ᣬ��pH����1����ͼ�п�ʼpH=1����A����B����������Һ��ͨ�백����Ӧ����ǿ���������泥���������ǿ�������ܽӽ�0����ͼ������B����
C��ʯīת��Ϊ���ʯ������������֪ʯī�����ͣ���ʯī�Ƚ��ʯ�ȶ�����C��ȷ��
D��t1ʱ������Ӧ���ʼ�С��Ȼ����������ܼ�СSO2��Ũ�ȵ�ͬʱ��С�� SO3��Ũ�ȣ���D����
��ѡC��
�����㾫�������ڱ��⿼�������к͵ζ�����Ҫ�˽��к͵ζ�ʵ��ʱ��������ˮϴ���ĵζ������ñ�Һ��ϴ����װ��Һ�����ô���Һ��ϴ������ȡҺ�壻�ζ��ܶ���ʱ�ȵ�һ�����Ӻ��ٶ������۲���ƿ����Һ��ɫ�ĸı�ʱ���ȵȰ������ɫ�����Ϊ�ζ��յ���ܵó���ȷ�𰸣�

 ��У����ϵ�д�
��У����ϵ�д�����Ŀ��������ԭ�ζ�ԭ��ͬ�к͵ζ�ԭ�����ƣ�Ϊ�˲ⶨijδ֪Ũ�ȵ�NaHSO3��Һ��Ũ�ȣ�����0.1000mol/L������KMnO4��Һ���еζ����ش��������⣺
��1����ƽ���ӷ���ʽ��MnO4��+HSO3��+H+����Mn2++SO42��+H2O
��2����KMnO4���еζ�ʱ��KMnO4��ҺӦװ���У��жϵζ��յ�������� ��
��3�����в����ᵼ�²ⶨ���ƫ�ߵ���
A.δ�ñ�Ũ�ȵ�����KMnO4��Һ��ϴ�ζ���
B.ʢװδ֪Һ����ƿ������ˮϴ����δ�ô���Һ��ϴ
C.�ζ�ǰ�ζ��ܼ��첿��������
D.�۲����ʱ���ζ�ǰ���ӣ��ζ�����
��4�������±��вⶨ��ʵ�����ݣ�����KMnO4��Һ�����ƽ��ֵΪmL��NaHSO3��Һ�����ʵ���Ũ��Ϊmol/L�����ݾ�ȷ��0.1��
ʵ���� | ����NaHSO3��Һ�����/mL | KMnO4��Һ�����/mL |
1 | 20.00 | 15.98 |
2 | 20.00 | 17.00 |
3 | 20.00 | 16.02 |