题目内容
拆开1mol化学键所吸收的能量是该化学键的键能,它的大小可以衡量化学键的强弱.
下列说法中错误的是( )
| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能/kJ?mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
| A、SiCl4的熔点比SiC低 |
| B、拆开1 mol晶体硅中的化学键所吸收的能量为176kJ |
| C、HCl的熔点比H2高 |
| D、拆开1 mol晶体SiC中的化学键所吸收的能量为1388kJ |
分析:A.SiCl4的是分子晶体,SiC是原子晶体,熔点原子晶体>分子晶体;
B.晶体硅中1个Si原子与周围的4个Si形成正四面体空间网状结构,每个Si原子形成4个Si-Si键,每个Si-Si键为1个
Si原子通过
Si-Si键,所以1mol晶体硅中含有Si-Si键为1mol×4×
=2mol;
C.范德华力越大熔沸点越高;
D.晶体SiC中1个Si原子与周围的4个C形成正四面体空间网状结构,每个Si原子形成4个Si-C键,每个Si-C键为1个Si原子通过
Si-C键,所以1mol晶体硅中含有Si-C键为1mol×4×
=2mol.
B.晶体硅中1个Si原子与周围的4个Si形成正四面体空间网状结构,每个Si原子形成4个Si-Si键,每个Si-Si键为1个
Si原子通过
| 1 |
| 2 |
| 1 |
| 2 |
C.范德华力越大熔沸点越高;
D.晶体SiC中1个Si原子与周围的4个C形成正四面体空间网状结构,每个Si原子形成4个Si-C键,每个Si-C键为1个Si原子通过
| 1 |
| 2 |
| 1 |
| 2 |
解答:解:A.SiCl4的是分子晶体,SiC是原子晶体,熔点原子晶体>分子晶体,所以SiCl4的熔点比SiC熔点低,故A正确;
B.晶体硅中1个Si原子与周围的4个Si形成正四面体空间网状结构,每个Si原子形成4个Si-Si键,每个Si-Si键为1个
Si原子通过
Si-Si键,所以1mol晶体硅中含有Si-Si键为1mol×4×
=2mol,拆开1mol晶体硅中的化学键所吸收的能量为176kJ/mol×2mol=352kJ,故B错误;
C.相对分子质量越大,范德华力越大,熔沸点越高,故C正确;
D.晶体硅中1个Si原子与周围的4个C形成正四面体空间网状结构,每个Si原子形成4个Si-C键,每个Si-C键为1个Si原子通过
Si-C键,所以1mol晶体硅中含有Si-C键为1mol×4×
=2mol,拆开1mol晶体硅中的化学键所吸收的能量为347kJ/mol×2mol=694kJ,故D正确.
故选B.
B.晶体硅中1个Si原子与周围的4个Si形成正四面体空间网状结构,每个Si原子形成4个Si-Si键,每个Si-Si键为1个
Si原子通过
| 1 |
| 2 |
| 1 |
| 2 |
C.相对分子质量越大,范德华力越大,熔沸点越高,故C正确;
D.晶体硅中1个Si原子与周围的4个C形成正四面体空间网状结构,每个Si原子形成4个Si-C键,每个Si-C键为1个Si原子通过
| 1 |
| 2 |
| 1 |
| 2 |
故选B.
点评:本题考查晶体类型与性质、键能概念及键能键长的运用等,难度中等,BD选项为易错点,要根据晶体结构判断1mol晶体硅中含有Si-Si键为2mol.

练习册系列答案
相关题目
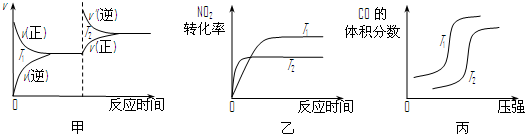
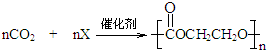 ,则X的结构简式为
,则X的结构简式为