题目内容
已知下列热化学方程式:
 CH4(g)+O2(g)=
CH4(g)+O2(g)=
 C02(g)+H2O(1);∆H
=-445.15kJ·mol-1
C02(g)+H2O(1);∆H
=-445.15kJ·mol-1
CH4(g)+ O2(g)=CO(g)+2H2O(1);
∆H=-607.3kJ·mol-1
O2(g)=CO(g)+2H2O(1);
∆H=-607.3kJ·mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(1); ∆H =-890.3 kJ·mol-1
CH4(g)+2O2(g)=CO2(g)十2H2O(g); ∆H =-802.3 kJ·mol-1
则CH4的燃烧热为
A.445.15 kJ·mol-1 B.607.3 kJ·mol-1 C.890.3 kJ·mol-1 D.802.3 kJ·mol-1
【答案】
C
【解析】燃烧热是在一定条件下,1mol可燃物完全燃烧,生成稳定的氧化物时所放出的热量,水的稳定状态是液态,所以正确的答案选C。

练习册系列答案
相关题目
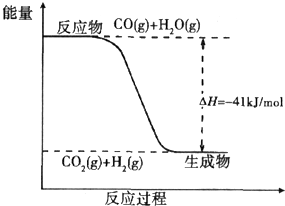 煤炭可以转化为清洁能源和化工原料.
煤炭可以转化为清洁能源和化工原料.