题目内容
在平衡体系中:H2S?H++HS-,HS-?H++S2-,增大溶液的pH值时,则c(S2-)变化正确的是( )
| A、增大 | B、可能增大也可能减小 |
| C、减小 | D、不变 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:H2S溶液中存在H2S?HS-+H+,HS-?S2-+H+,采取措施使pH增大,可加入NaOH、水解呈碱性的物质或加水稀释,以此解答该题.
解答:
解:H2S溶液中存在H2S?HS-+H+,HS-?S2-+H+,使pH增大,应使c(H+)减小,如加入NaOH、水解呈碱性的物质,则c(S2-)增大,如加水稀释,则c(S2-)减小,
所以c(S2-)可能增大也可能减小;
故选B.
所以c(S2-)可能增大也可能减小;
故选B.
点评:本题考查弱电解质的电离,题目难度不大,注意把握影响弱电解质的电离平衡的因素,答题时注意pH增大可能措施.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列实验设计和结论正确的是( )
| A、某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性 |
| B、向0.1mol?L-1的FeSO4溶液中滴加少量酸性KMnO4溶液,KMnO4溶液褪色,说明Fe2+具有漂白性 |
| C、将碘水倒入分液漏斗中,加入适量乙醇,振荡后静置,可降碘萃取到乙醇中 |
| D、向锌粒与稀H2SO4的反应溶液中加入CuSO4,产生气泡的速度加快,说明CuSO4对此反应有催化作用 |
在CH3COOH溶液中存在如下平衡:CH3COOH?CH3COO-+H+,要使溶液中的氢离子浓度减少应加入的物质是( )
| A、少量HCl |
| B、少量NaCl |
| C、CH3COONa |
| D、少量冰醋酸 |
一定条件下a mol CO2通过足量Na2O2,将所得气体与b mol NO混合,得c mol气体.若不考虑NO2的二聚反应,则关于c的判断错误的是( )
| A、若a<b时,c>(a+b) |
| B、若a<b时,c<(a+b) |
| C、若a>b时,c=(a+b) |
| D、若a=b时,c=(a+b) |
下列实验方案与实验结论符合或能达到实验目的是( )
A、 探究NaHCO3的热稳定性 |
B、 用铜和浓硝酸制取少量NO2 |
C、 实验室制取Cl2 |
D、 白色沉淀为BaSO4 |
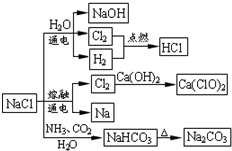 NaCl是一种化工原料,可以制备一系列物质(如图所示).下列说法正确的是( )
NaCl是一种化工原料,可以制备一系列物质(如图所示).下列说法正确的是( )| A、常温下干燥Cl2能用钢瓶贮运,所以Cl2与铁不反应 |
| B、25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| C、源石灰乳与Cl2的反应中Cl2既是氧化剂,又是还原剂 |
| D、图中所示转化反应都是氧化还原反应 |
常温下PH=2的A酸溶液和pH=12的B碱溶液等体积混合后,溶液的pH一定小于7,则A、B可能 为( )
| A、强酸、强碱 |
| B、弱酸、弱碱 |
| C、强酸、弱碱 |
| D、弱酸、强碱 |
已知室温时0.1mol/L某一元酸HA在水中有0.1%发生电离,叙述错误的是( )
| A、该溶液的pH=4 |
| B、升高温度,溶液的KW增大 |
| C、此酸的电离平衡常数约为1×10-7 |
| D、该溶液里不存在HA分子 |