题目内容
已知合成氨反应的浓度数据如下:
当用氢气浓度的改变量来表示该化学反应速率时,其速率为( )
| 方程式 | N2+3H2?2NH3 | ||
| 起始浓度/mol?L-1 | 1.0 | 3.0 | 0 |
| 3秒末浓度/mol?L-1 | 0.6 | 1.8 | 0.8 |
| A、0.2 mol?L-1?s-1 |
| B、0.3 mol?L-1?s-1 |
| C、0.4 mol?L-1?s-1 |
| D、0.6mol?L-1?s-1 |
考点:反应速率的定量表示方法
专题:化学反应速率专题
分析:计算3s内氢气的浓度变化量,再根据c=
计算3s内用氢气表示的平均反应速率.
| △c |
| △t |
解答:
解:3s内氢气的浓度变化量=3.0mol/L-1.8mol/L=1.2mol/L,
故2s内用氢气表示的平均反应速率=
=0.4mol/(L.s)
故选C.
故2s内用氢气表示的平均反应速率=
| 1.2mol/L |
| 3s |
故选C.
点评:本题考查化学反应速率的计算,比较基础,注意对公式的理解与灵活应用.

练习册系列答案
相关题目
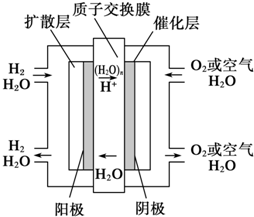 为体现“城市让生活更美好”的主题,上海市政府承诺世博园区内交通“零排放”、园区周边交通“低排放”.2010年4月15日新能源车交车仪式在世博园举行,该车装着“绿色心脏”--质子交换膜燃料电池,其工作原理如图所示,下列叙述正确的是( )
为体现“城市让生活更美好”的主题,上海市政府承诺世博园区内交通“零排放”、园区周边交通“低排放”.2010年4月15日新能源车交车仪式在世博园举行,该车装着“绿色心脏”--质子交换膜燃料电池,其工作原理如图所示,下列叙述正确的是( )| A、通入氧气的电极发生氧化反应 | ||||
| B、通入氢气的电极为正极 | ||||
C、总反应式为O2+2H2
| ||||
| D、正极的电极反应式为O2+4H++4e-═2H2O |
下列说法正确的是( )
A、 的名称为2-羟基丁烷 的名称为2-羟基丁烷 |
B、 能使KMnO4溶液褪色,说明苯环与甲基相连的碳碳单键变得活泼,被KMnO4氧化而断裂 能使KMnO4溶液褪色,说明苯环与甲基相连的碳碳单键变得活泼,被KMnO4氧化而断裂 |
C、化合物 的分子式为C13H10O4N2 的分子式为C13H10O4N2 |
D、高聚物脲醛树脂 的合成单体之一是CH3OH 的合成单体之一是CH3OH |
在化学上,常用CaH2作为制取氢气的药剂,有关反应的化学方程式为:CaH2+2H2O=Ca(OH)2+2H2↑,在这个反应中( )
| A、CaH2是氧化剂 |
| B、电子转移数目为4e- |
| C、Ca(OH)2是氧化产物 |
| D、氧化产物和还原产物物质的量之比是1:1 |
下列关于胶体的叙述不正确的是( )
| A、胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9~10-7m之间 |
| B、光线透过胶体时,胶体中可发生丁达尔效应 |
| C、NaCl溶液和Fe(OH)3胶体中的分散质的微粒都是分子 |
| D、Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的 |
2mol铝分别与足量盐酸和氢氧化钠溶液反应,消耗的HCl和NaOH物质的量之比为( )
| A、1:1 | B、2:1 |
| C、3:1 | D、1:3 |
金刚石和石墨是碳元素的两种结构不同的单质(同素异形体).在100KPa时,1mol石墨转化为金刚石,要吸收1.895KJ的热能.据此,试判断在100KPa压强下,下列结论正确的是( )
| A、金刚石比石墨稳定 |
| B、石墨比金刚石稳定 |
| C、1mol石墨比1mol金刚石的总能量高 |
| D、1mol石墨和1mol 金刚石的总能量一样多 |
下列关于浓硫酸和浓硝酸的叙述正确的是( )
| A、浓硫酸具有吸水性,因而能使蔗糖炭化 |
| B、久置的浓硝酸会发黄,是因为HNO3不稳定,分解产生的NO2溶于其中 |
| C、常温下,浓硫酸和浓硝酸均可以与铜反应,放出气体 |
| D、常温下可用铁制容器运输浓硫酸和浓硝酸,是因为它们与铁不反应 |