题目内容
1.常温下,下列各组离子一定能大量共存的是( )| A. | 在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- | |
| B. | 在含有大量H+溶液中:Na+、K+、AlO2-、CO32- | |
| C. | 在含有大量OH-溶液中:CO32-、Na+、SO42-、NO3- | |
| D. | 在酸性的溶液中:K+、I-、Cl-、NO3- |
分析 A.离子之间结合生成络合离子;
B.离子之间结合生成沉淀、气体、水等;
C.碱性溶液中该组离子之间不反应;
D.离子之间发生氧化还原反应.
解答 解:A.Fe3+、SCN-结合生成络合离子,不能大量共存,故A错误;
B.H+、AlO2-结合生成沉淀,H+、CO32-结合生成气体、水,不能大量共存,故B错误;
C.碱性溶液中该组离子之间不反应,可大量共存,故C正确;
D.H+、I-、NO3-发生氧化还原反应,不能大量共存,故D错误;
故选C.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重氧化还原反应、复分解反应的离子共存考查,注意习题的限制条件,题目难度不大.

练习册系列答案
相关题目
12.近年来,“地沟油”的处理成为一个与食品安全密切相关的话题.据报道,2013年4月24日,东航首次成功进行了由地沟油生产的生物航空燃油的验证飞行.下列方法中,能区别地沟油(餐饮废弃油)与矿物油(汽油、煤油、柴油等)的方法是( )
| A. | 加入水中,浮在水面上的是地沟油 | |
| B. | 测定沸点,有固定沸点的是矿物油 | |
| C. | 点燃,能燃烧的是矿物油 | |
| D. | 加入含酚酞的氢氧化钠溶液,加热,红色变浅或消失的是地沟油 |
9.下表为各物质中所含的杂质以及除去这些杂质选用的试剂或操作方法,正确的是( )
| 物质 | 杂质 | 试剂或方法 | |
| A | 碘水 | Br2 | 乙醇、萃取 |
| B | FeCl3溶液 | CuCl2 | Fe |
| C | Fe2O3 | Al2O3 | 盐酸 |
| D | NaHCO3溶液 | Na2CO3 | 通入过量的CO2 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
16.下列实验操作正确且能达到实验目的是( )
| 实验目的 | 操作 | |
| A | 比较水和乙醇中羟基氢的活泼性强弱 | 用金属钠分别与水和乙醇反应 |
| B | 欲证明CH2=CHCHO中含有碳碳双键 | 滴入KMnO4酸性溶液,看紫红色是否褪去 |
| C | 确定溴乙烷中含有溴元素 | 与NaOH溶液共热,再往混合液中滴加AgNO3溶液,观察是否有浅黄色沉淀生成 |
| D | 欲除去苯中混有的苯酚 | 向混合液中加入浓溴水,充分反应后,过滤 |
| A. | A | B. | B | C. | C | D. | D |
6.今有高聚物…-CH2-CH(COOCH2CH3)-CH2-CH(COOCH2CH3)-CH2-CH(COOCH2CH3)-…,下列分析正确的是( )
| A. | 其单体是CH2=CH2和 H-CO-O-CH2CH3 | |
| B. | 它是缩聚反应的产物 | |
| C. | 其链节是 CH3-CH2-CO-O-CH2CH3 | |
| D. | 其单体是 CH2=CH-CO-O-CH2CH3 |
13. 某稀硫酸和稀硝酸的混合溶液200mL,将其分成两等份.向第一份中逐渐加入铜粉,最多能溶解19.2g(假设硝酸仅被还原为N0气体,下同).向第二份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,将其分成两等份.向第一份中逐渐加入铜粉,最多能溶解19.2g(假设硝酸仅被还原为N0气体,下同).向第二份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
 某稀硫酸和稀硝酸的混合溶液200mL,将其分成两等份.向第一份中逐渐加入铜粉,最多能溶解19.2g(假设硝酸仅被还原为N0气体,下同).向第二份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,将其分成两等份.向第一份中逐渐加入铜粉,最多能溶解19.2g(假设硝酸仅被还原为N0气体,下同).向第二份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )| A. | 原混合溶液中NO3-的物质的量为0.4 mol | |
| B. | OA段、BC段产生的气体分别是N0、H2 | |
| C. | 第二份溶液中最终溶质为FeS04 | |
| D. | 原混合溶液中H2S04的浓度为5 mol•L-1 |
10.能说明苯分子苯环的平面正六边形结构中,碳碳键不是单双键交替排布的事实是( )
| A. | 苯不能使溴水褪色 | B. | 苯能与H2发生加成反应 | ||
| C. | 苯的邻位二元取代物只有一种 | D. | 苯的对位二元取代物只有一种 |
11.化学与人类生活、社会可持续发展密切相关,下列说法正确的是( )
| A. | “天宫一号”中使用的碳纤维,是一种纤维素 | |
| B. | 回收制革工厂的边角皮料生产食用明胶,加工成医用胶囊或做食品增稠剂 | |
| C. | 氯化汞(HgCl2)的稀溶液可用于手术器械消毒,因为它会使蛋白质变性,杀菌消毒 | |
| D. | 蛋白质、淀粉、纤维素、油脂、葡萄糖等都能在人体内水解并提供能量 |
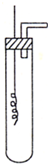 某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如图所示的
某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如图所示的