题目内容
同温同压下,同体积的CO和CO2,下列说法不正确的是( )
| A、分子数之比等于1:1 |
| B、原子数之比等于3:2 |
| C、质量之比等于7:11 |
| D、质子数之比等于7:11 |
考点:物质的量的相关计算
专题:计算题
分析:同温同压下,相同体积的气体含有相同分子数目、相同的物质的量,结合每个分子含有原子数目、质子数目计算原子总数之比、质子总数之比,根据m=nM判断质量之比
解答:
解:A.同温同压下,同体积的CO和CO2含有相同分子数目,故A正确;
B.同温同压下,同体积的CO和CO2含有相同分子数目,则含有原子数之比等于2:3,故B错误;
C.同温同压下,同体积的CO和CO2的物质的量相等,根据m=nM,可知二者质量之比=28g/mol:44g/mol=7:11,故C正确;
D.同温同压下,同体积的CO和CO2含有相同分子数目,则含有质子数之比等于14:22=7:11,故D正确,
故选B.
B.同温同压下,同体积的CO和CO2含有相同分子数目,则含有原子数之比等于2:3,故B错误;
C.同温同压下,同体积的CO和CO2的物质的量相等,根据m=nM,可知二者质量之比=28g/mol:44g/mol=7:11,故C正确;
D.同温同压下,同体积的CO和CO2含有相同分子数目,则含有质子数之比等于14:22=7:11,故D正确,
故选B.
点评:本题考查阿伏伽德罗定律、微粒数目计算,比较基础,注意根据PV=nRT理解阿伏伽德罗定律及其推论.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列关于晶体的说法一定正确的是( )
| A、分子晶体中都存在共价键 |
| B、金属晶体的熔点都比分子晶体的熔点高 |
| C、SiO2晶体中每个硅原子与两个氧原子以共价键相结合 |
D、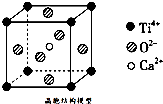 某物质晶胞结构如图,该物质的化学式为CaTiO3(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶点) |
05L 1mol/L的FeCl3与0.2L 1mol/L的KCl 溶液中,Cl-的物质的量浓度之比为( )
| A、5:2 | B、1:1 |
| C、3:1 | D、1:3 |
下列说法正确的是( )
| A、在标准状况下,1mol水的体积是22.4L |
| B、1molH2所占的体积一定是22.4L |
| C、在标准状况下,NA个任何分子所占的体积约为22.4L |
| D、在标准状况下,总质量为28g的N2和CO的混合气体,其体积约为22.4L |
下列说法正确的是( )
| A、可用丁达尔效应区分胶体与溶液 |
| B、生石灰与水混合过程只发生物理变化 |
| C、臭氧是由三个氧原子构成的化合物 |
| D、CuSO4?H2O是一种混合物 |
短周期元素R的最高价氧化物对应的水化物的化学式为HxROy,其气态氢化物的化学式为HzR(或RHz),已知1mol HxROy比1mol HzR的质量多64克,下列说法不正确的是( )
| A、有多种元素符合本题条件 |
| B、符合本题的HxROy有一元酸和多元酸 |
| C、z与x的数值相等 |
| D、R可能是第二周期元素 |