题目内容
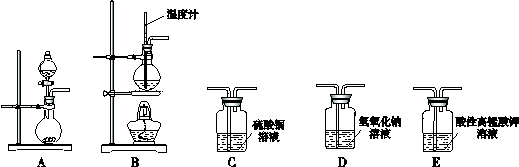
在实验室利用下列装置,可制备某些气体并验证其化学性质.
完成下列表格:
(3)D装置中氢氧化钠溶液的作用 .

完成下列表格:
| 序号 | 气体 | 装置连接顺序(填字母) | 制备反应的化学方程式 |
| (1) | 乙烯 | B→D→E | |
| (2) | 乙炔 |
考点:实验装置综合
专题:实验设计题
分析:(1)实验室制取乙烯,需要加热到170℃,应该选择B装置,反应中会发生副反应生成二氧化硫,必须用氢氧化钠溶液除去,所以选择D装置除质;最后用高锰酸钾溶液检验乙烯的性质;
(2)碳化钙与与水反应生成乙炔,选A为反应装置,然后选C为除杂装置,选E为性质实验装置;
(3)NaOH溶液的作用为除去.
(2)碳化钙与与水反应生成乙炔,选A为反应装置,然后选C为除杂装置,选E为性质实验装置;
(3)NaOH溶液的作用为除去.
解答:
解:(1)在实验室中制取乙烯,需要加热到170℃,应该选择B装置,反应中会发生副反应生成二氧化硫,必须用氢氧化钠溶液除去,所以选择D装置除去二氧化硫、二氧化碳杂质;最后用高锰酸钾溶液检验乙烯的性质,所以连接顺序为:B→D→E,实验室利用乙醇能发生消去反应制乙烯的反应为CH3-CH2-OH
CH2=CH2↑+H2O,
故答案为:CH3-CH2-OH
CH2=CH2↑+H2O;
(2)碳化钙与与水反应生成乙炔,选A为反应装置,然后选C为除杂装置,选E为性质实验装置,则装置的顺序为A→C→E,制备乙炔的反应为CaC2+2H2O→CH≡CH↑+Ca(OH)2,故答案为:A→C→E;CaC2+2H2O→CH≡CH↑+Ca(OH)2;
(3)由(1)可知,D装置中氢氧化钠溶液的作用是除二氧化碳和二氧化硫,故答案为:除二氧化碳和二氧化硫.
| 浓H2SO4 |
| 170℃ |
故答案为:CH3-CH2-OH
| 浓H2SO4 |
| 170℃ |
(2)碳化钙与与水反应生成乙炔,选A为反应装置,然后选C为除杂装置,选E为性质实验装置,则装置的顺序为A→C→E,制备乙炔的反应为CaC2+2H2O→CH≡CH↑+Ca(OH)2,故答案为:A→C→E;CaC2+2H2O→CH≡CH↑+Ca(OH)2;
(3)由(1)可知,D装置中氢氧化钠溶液的作用是除二氧化碳和二氧化硫,故答案为:除二氧化碳和二氧化硫.
点评:本题考查实验装置综合和气体的制备,为高频考点,把握制备原理及实验装置的作用为解答的关键,侧重分析及实验能力的考查,题目难度不大.

练习册系列答案
相关题目
下列解释正确的是( )
| A、摩尔是国际七个基本物理量之一 |
| B、物质的量是一个独立的专有名词 |
| C、摩尔是物质的质量的单位 |
| D、摩尔质量等于相对分子质量 |
下列电离方程式错误的是( )
| A、含H2CO3的溶液:H2CO3═2H++CO32- |
| B、极少量Fe(OH)3溶于水:Fe(OH)3?Fe3++3OH- |
| C、醋酸溶液:CH3COOH??H++CH3COO- |
| D、NaHSO4溶于水:NaHSO4═Na++H++SO42- |
将含有硝酸钙和硫酸镁杂质的硝酸钾溶于水,加入某些试剂,结合过滤、蒸发等操作,可得到纯净的硝酸钾.加入试剂的顺序正确的是( )
| A、K2CO3、Ba(NO3)2、KOH、HNO3 |
| B、Ba(NO3)2、KOH、HNO3、K2CO3 |
| C、KOH、K2CO3、Ba(NO3)2、HNO3 |
| D、Ba(NO3)2、KOH、K2CO3、HNO3 |
对于某些离子的检验及结论一定正确的是( )
| A、加入稀盐酸产生气体,将气体通入澄清石灰水,溶液变浑浊,可能有CO32- |
| B、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| C、加硝酸银溶液产生白色沉淀,一定有Cl- |
| D、加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |