题目内容
3. 质量相等的C4H6和N2气体在容积可变的容器中的体积和温度的关系如图所示.
质量相等的C4H6和N2气体在容积可变的容器中的体积和温度的关系如图所示.(1)C4H6和N2的摩尔质量之比为27:14
(2)B表示C4H6气体
(3)若压强始终为1.01×105Pa,则气体A的物质的量为0.2mol,质量为5.6g.
分析 (1)摩尔质量以g/mol为单位时,与其相对分子质量成正比;
(2)相同温度下气体体积与物质的量成正比,结合C4H6和N2的摩尔质量判断;
(3)0℃、1.01×105Pa为标准状况下,A为氮气,根据n=$\frac{V}{{V}_{m}}$计算出氮气的物质的量,根据m=nM计算出氮气的质量.
解答 解:(1)C4H6和N2的摩尔质量之比=54g/mol:28g/mol=27:14,
故答案为:27:14;
(2)质量相等的C4H6和N2气体,根据n=$\frac{m}{M}$可知C4H6和N2的物质的量之比与摩尔质量成反比,则N2的物质的量较大,C4H6的物质的量减小;温度相同时,容器体积与气体物质的量成正比,根据图象可知,温度相同时,A的体积较大,则A为N2,B为C4H6,
故答案为:C4H6;
(3)0℃、1.01×105Pa为标准状况下,A表示的是N2,根据图象可知其体积为4.48L,标准状况下4.48L N2的物质的量为:$\frac{4.48L}{22.4L/mol}$=0.2mol,质量为:28g/mol×0.2mol=5.6g,
故答案为:0.2mol;5.6g.
点评 本题考查了物质的量的计算,题目难度中等,明确相同温度下气体物质的量与容器容积成正比为解答关键,试题有利于提高学生的分析能力及化学计算能力.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
16.下列各组混合物中,能用分液漏斗进行分离的是( )
| A. | 醋酸和水 | B. | 水和四氯化碳 | C. | 碘和四氯化碳 | D. | 汽油和植物油 |
13.下列说法不正确的是( )
| A. | 与Na反应时,乙醇的反应速率比水慢 | |
| B. | 除去乙烷中混有的少量乙烯的方法是通入溴水 | |
| C. | 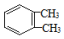 和 和 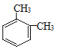 是同一种物质,说明苯分子中的碳碳键不是单双键交替的 是同一种物质,说明苯分子中的碳碳键不是单双键交替的 | |
| D. | 苯不能使酸性高锰酸钾溶液褪色,所以苯不能发生氧化反应 |
15.甲酸中含有醛基与羧基两种官能团,是一种特殊的酸,它与溴水可以发生如下反应:Br2(aq)+HCOOH(aq)→2HBr(aq)+CO2(g).生成CO2的初始速率与反应物起始浓度关系如下表:
现将0.02mol•L-1溴水和0.02mol•L-1 HCOOH溶液等体积混合,此时生成CO2的初始速率(单位:mol•L-1•s-1)应为( )
| 实验序号 | 起始浓度 | CO2(g)起始速率/mol•L-1•S-1 | |
| c(Br2) | c(HCOOH) | ||
| 1 | 0.01 | 0.02 | 2.0×10-6 |
| 2 | 0.02 | 0.04 | 8.0×10-6 |
| 3 | 0.03 | 0.02 | 6.0×10-6 |
| A. | 1.0×10-6 | B. | 1.0×10-7 | C. | 4.0×10-6 | D. | 5.0×10-7 |
12.下列说法正确的是( )
| A. | 记录Na2S2O3与稀硫酸的反应时间,应从溶液混合时开始计时,到刚出现浑浊结束 | |
| B. | 将少量溴乙烷与氢氧化钾水溶液充分反应,应先加硝酸酸化,然后在试管中加入AgNO3溶液,观察是否出现浅黄色沉淀,该实验可检验溴乙烷中是否含有溴元素 | |
| C. | 将两块未擦去氧化膜的铝片分别投入1mol•L-1CuSO4和1mol•L-1CuCl2溶液中,铝片表面都观察不到明显的反应现象 | |
| D. | 人体吸入氯气、氯化氢气体时,可吸入少量酒精或乙醚的混合气体解毒;氨气、溴中毒休克时要马上进行人工呼吸 |
13.足量下列溶液与相同质量的铝反应放出氢气,消耗溶质物质的量最少的是( )
| A. | NaOH溶液 | B. | 稀硫酸 | C. | 盐酸 | D. | Ba(OH)2溶液 |
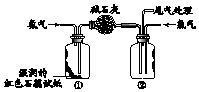 某同学利用图所示装置探究氨气的性质.
某同学利用图所示装置探究氨气的性质.