题目内容
19.烷烃A只可能有三种一氯取代产物B、C和D.C的结构简式如图所示 ,B和D分别与强碱的醇溶液共热,都只能得到有机化合物E.以上反应及B的进一步反应如下图所示.请回答:
,B和D分别与强碱的醇溶液共热,都只能得到有机化合物E.以上反应及B的进一步反应如下图所示.请回答:
(1)A的结构简式是(CH3)3CCH2CH3.
(2)H的结构简式是(CH3)3CCH2COOH.
(3)B转变为F的反应属于取代 反应,B转变为E的反应属于消去 反应(填反应类型名称).
(4)系统命名法命名E3,3-二甲基-1-丁烯
(5)1.16gH与足量NaHCO3作用,标况下可得CO2的体积是224 mL.
分析 烷烃A只可能有三种一氯取代产物B、C和D,C的结构简式是(CH3)2C(CH2CH3)CH2Cl,故A为(CH3)3CCH2CH3,B和D分别与强碱的醇溶液共热,都只能得到有机化合物E,故E为(CH3)3CCH=CH2,B在氢氧化钠水溶液下生成F,F为醇,F氧化生成G,G能与银氨溶液反应,G含有醛基-CHO,故B为(CH3)3CCH2CH2Cl,F为(CH3)3CCH2CH2OH,G为(CH3)3CCH2CHO,H为(CH3)3CCH2COOH,D为(CH3)3CCH2ClCH3),以此解答该题.
解答 解:烷烃A只可能有三种一氯取代产物B、C和D,C的结构简式是(CH3)2C(CH2CH3)CH2Cl,故A为(CH3)3CCH2CH3,B和D分别与强碱的醇溶液共热,都只能得到有机化合物E,故E为(CH3)3CCH=CH2,B在氢氧化钠水溶液下生成F,F为醇,F氧化生成G,G能与银氨溶液反应,G含有醛基-CHO,故B为(CH3)3CCH2CH2Cl,F为(CH3)3CCH2CH2OH,G为(CH3)3CCH2CHO,H为(CH3)3CCH2COOH,D为(CH3)3CCH2ClCH3),
(1)由上述分析可知,A的结构简式是(CH3)3CCH2CH3,故答案为:(CH3)3CCH2CH3;
(2)由上述分析可知,H的结构简式是(CH3)3CCH2COOH,故答案为:(CH3)3CCH2COOH;
(3)B转变为F是(CH3)3CCH2CH2Cl在氢氧化钠水溶液下生成(CH3)3CCH2CH2OH,属于取代反应,B转变为E是(CH3)3CCH2CH2Cl在氢氧化钠醇溶液下发生消去反应生成(CH3)3CCH=CH2,故答案为:取代;消去;
(4)E为(CH3)3CCH=CH2,名称为3,3-二甲基-1-丁烯,故答案为:3,3-二甲基-1-丁烯;
(5)1.16g(CH3)3CCH2COOH的物质的量为$\frac{1.16g}{116g/mol}$=0.01mol,由(CH3)3CCH2COOH+NaHCO3=(CH3)3CCH2COONa+H2O+CO2↑可知,生成CO2的物质的量为0.01mol,二氧化碳的体积是0.01mol×22.4L/mol=0.224L=224mL,故答案为:224.
点评 本题考查有机物的推断,涉及烷、卤代烃、醇、醛、羧酸的性质与转化等,难度中等,根据A的卤代产物推断A的结构是关键,然后利用顺推法推断结合有机物的反应特点和含有的官能推断.

①硅酸钠可用于制备木材防火剂
②硅是构成一些岩石和矿物的基本元素
③高纯度的硅单质广泛用于制作光导纤维
④陶瓷,水晶,玻璃等是人类应用很早的硅酸盐材料.
| A. | ①② | B. | ①③ | C. | ②④ | D. | ③④ |

| A. | 图1中,插入海水中的铁棒,越靠近底端腐蚀越严重 | |
| B. | 图2中,正极附近无明显现象 | |
| C. | 图3中,燃气灶的中心部位容易生锈,主要是由于高温下铁发生化学腐蚀 | |
| D. | 图4中,用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块相当于原电池的正极 |
| A. | 氯仿 | B. | 汽油 | C. | 硝基苯 | D. | 甲醇 |
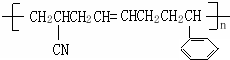
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
| A. | 水与冰 | B. | O2与O3 | C. | 丁烷和正丁烷 | D. | 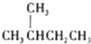 与 与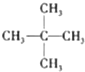 |
| A. | 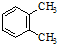 与 与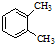 是同分异构体 是同分异构体 | |
| B. | 苯可以发生加成反应 | |
| C. | 可通过萃取的方法,从煤中提取苯 | |
| D. | 向2mL苯中加入1mL酸性高锰酸钾溶液,震荡后静置,可观察到液体分层,上层呈紫红色 |
| A. | 分散质粒子直径在1~100nm之间 | B. | 可用丁达尔效应区别这两种物质 | ||
| C. | 能用过滤的方法将它们分离 | D. | 都呈红褐色 |
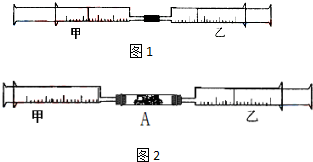 如图1所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质缓缓地压到甲针筒内,进行下表所列的不同实验(气体体积在常温常压下测定).
如图1所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质缓缓地压到甲针筒内,进行下表所列的不同实验(气体体积在常温常压下测定).| 实验序号 | 甲针筒内物质 | 乙针筒内物质 | 甲针筒的现象 |
| 1 | 40mL HCl | 40mL NH3 | 产生白烟 |
| 2 | 40mL Cl2 | 10mL 水 | 剩余气体为20mL |
| 3 | 30mL NO | 15mL O2 | |
| 4 | 20mL AlCl3溶液 | 10mL NaOH溶液 | 生成白色沉淀,后消失 |
(2)由实验2可知,常温常压下氯气在水中的溶解度为1体积水溶解2体积氯气.
(3)实验3 反应后甲针筒内气体的体积为15ml~30ml.
(4)实验4中,AlCl3溶液浓度为0.1mol/L,如果最后白色沉淀全部消失,则NaOH溶液浓度至少为0.8mol/L.
(5)将上述装置做以下改进:在甲、乙针筒之间连接一段硬质玻璃管,如图2.在A处装一种浅黄色的粉末,乙针筒内是一种常见的气体,甲针筒无气体.将乙针筒内气体压入甲针筒内,发现气体体积是原来的一半.A处的物质是Na2O2,甲针筒内的气体为O2.
(6)有学生用上述改进后的装置测定空气中氧气的体积分数(加热用酒精灯未画出).乙针筒内装有50mL空气.实验时,用酒精灯对A处物质进行加热,经反复慢慢推拉两针筒的活塞,反应完毕,恢复至室温,测得剩余气体为40.5mL.
1)A处的物质是c(选填编号).
a.碳粉 b.二氧化锰 c.铜粉 d.氧化铜
2)已知空气中氧气的体积分数为0.2,则该实验的相对误差为-5%.