题目内容
下列叙述正确的是
- A.将SO2通入BaCl2溶液中至饱和,将产生白色沉淀
- B.在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉仍不溶解
- C.浓HNO3、氯水、AgBr溶液、AgNO3溶液都应该保存在棕色玻璃瓶中
- D.工业上分别用电解融熔NaCl、MgCl2、AlCl3的方法制得金属Na、Mg、Al
C
分析:A.盐酸的酸性比亚硫酸的酸性强,将SO2通入BaCl2溶液中,无沉淀生成;
B.铜粉与稀硫酸不反应,铜粉与HNO3反应;
C.浓HNO3、氯水、AgBr溶液、AgNO3溶液见光分解;
D.工业上分别用电解融熔NaCl、MgCl2的方法制得金属Na、Mg,但Al不能通过电解AlCl3制得,因融熔AlCl3只有分子,没有离子.
解答:A.SO2通入BaCl2溶液中,假设有沉淀,则会生成盐酸,而盐酸的酸性比亚硫酸的酸性强,盐酸与亚硫酸钡反应生成BaCl2和SO2,故假设不成立,无沉淀生成.故A错误;
B.稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,此时溶液中有Cu(NO3)2电离出的硝酸根离子、稀硫酸电离出的氢离子,铜粉在溶液中相当于与稀硝酸反应.反应的离子方程式为:3Cu+8H++2NO3-=Cu2++2NO↑+4H2O.故B错误;
C.浓HNO3见光分解的方程式为:4HNO3NO3NO3 4NO2↑+O2↑+2H2O;
4NO2↑+O2↑+2H2O;
氯水中氯气与水反应:Cl2+H2O?HCl+HClO,生成的次氯酸见光分解的方程式为:2HClO 2HCl+O2↑;
2HCl+O2↑;
AgBr溶液见光分解的方程式为:2AgBrAgBr 2Ag+Br2;
2Ag+Br2;
AgNO3溶液见光分解的方程式为:2AgNO3AgNO3 2Ag+2NO2↑+O2↑所以都应该保存在棕色玻璃瓶中.故C正确;
2Ag+2NO2↑+O2↑所以都应该保存在棕色玻璃瓶中.故C正确;
D.工业上分别用电解融熔NaCl、MgCl2制得金属Na、Mg的方程式分别为:2NaCl 2Na+Cl2↑,MgCl2融熔电解
2Na+Cl2↑,MgCl2融熔电解 Mg+Cl2↑融熔AlCl3只有分子,没有离子,工业上用电解融熔的氧化铝制得铝,反应为:2Al2O3
Mg+Cl2↑融熔AlCl3只有分子,没有离子,工业上用电解融熔的氧化铝制得铝,反应为:2Al2O3 4Al+3O2↑.故D错误;
4Al+3O2↑.故D错误;
故选C.
点评:该题主要考查了工业上用电解制取金属单质的方法,考查了卤素、氮族元素及相关化合物的性质,关键在于明晰反应的原理.
分析:A.盐酸的酸性比亚硫酸的酸性强,将SO2通入BaCl2溶液中,无沉淀生成;
B.铜粉与稀硫酸不反应,铜粉与HNO3反应;
C.浓HNO3、氯水、AgBr溶液、AgNO3溶液见光分解;
D.工业上分别用电解融熔NaCl、MgCl2的方法制得金属Na、Mg,但Al不能通过电解AlCl3制得,因融熔AlCl3只有分子,没有离子.
解答:A.SO2通入BaCl2溶液中,假设有沉淀,则会生成盐酸,而盐酸的酸性比亚硫酸的酸性强,盐酸与亚硫酸钡反应生成BaCl2和SO2,故假设不成立,无沉淀生成.故A错误;
B.稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,此时溶液中有Cu(NO3)2电离出的硝酸根离子、稀硫酸电离出的氢离子,铜粉在溶液中相当于与稀硝酸反应.反应的离子方程式为:3Cu+8H++2NO3-=Cu2++2NO↑+4H2O.故B错误;
C.浓HNO3见光分解的方程式为:4HNO3NO3NO3
 4NO2↑+O2↑+2H2O;
4NO2↑+O2↑+2H2O;氯水中氯气与水反应:Cl2+H2O?HCl+HClO,生成的次氯酸见光分解的方程式为:2HClO
 2HCl+O2↑;
2HCl+O2↑;AgBr溶液见光分解的方程式为:2AgBrAgBr
 2Ag+Br2;
2Ag+Br2; AgNO3溶液见光分解的方程式为:2AgNO3AgNO3
 2Ag+2NO2↑+O2↑所以都应该保存在棕色玻璃瓶中.故C正确;
2Ag+2NO2↑+O2↑所以都应该保存在棕色玻璃瓶中.故C正确;D.工业上分别用电解融熔NaCl、MgCl2制得金属Na、Mg的方程式分别为:2NaCl
 2Na+Cl2↑,MgCl2融熔电解
2Na+Cl2↑,MgCl2融熔电解 Mg+Cl2↑融熔AlCl3只有分子,没有离子,工业上用电解融熔的氧化铝制得铝,反应为:2Al2O3
Mg+Cl2↑融熔AlCl3只有分子,没有离子,工业上用电解融熔的氧化铝制得铝,反应为:2Al2O3 4Al+3O2↑.故D错误;
4Al+3O2↑.故D错误;故选C.
点评:该题主要考查了工业上用电解制取金属单质的方法,考查了卤素、氮族元素及相关化合物的性质,关键在于明晰反应的原理.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
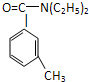 避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH
避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH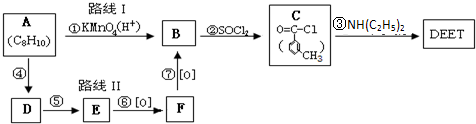
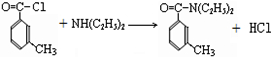
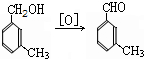
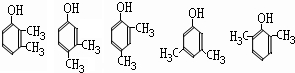 (任写2种)
(任写2种)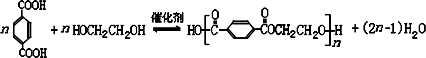
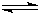 NH3?H2O+H+
NH3?H2O+H+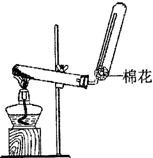 (2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.
(2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.