题目内容
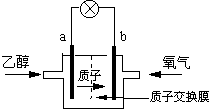 一种新型的乙醇电池,它用磺酸类质子溶剂.电池总反应为:C2H5OH+3O2→2CO2+3H2O,电池示意如图,下列说法正确的是( )
一种新型的乙醇电池,它用磺酸类质子溶剂.电池总反应为:C2H5OH+3O2→2CO2+3H2O,电池示意如图,下列说法正确的是( )| A、a极为电池的正极 |
| B、电池工作时电流由a极沿导线经灯泡再到b极 |
| C、电池负极的电极反应为:4H++O2+4e-=2H2O |
| D、电池工作时,1mol乙醇被氧化时就有12mol电子转移 |
考点:化学电源新型电池
专题:电化学专题
分析:A.在燃料电池中,燃料在负极发生失电子的反应;
B.在燃料电池中,电流在电路中从正极流向负极;
C.在燃料电池中,正极上是氧气得电子的还原反应,燃料在负极发生失电子的反应;
D.根据电池反应:C2H5OH+3O2=2CO2+3H2O,乙醇被氧化电极反应式为C2H5OH+3H2O-12e-=2CO2+12H+,反应转移电子数为12.
B.在燃料电池中,电流在电路中从正极流向负极;
C.在燃料电池中,正极上是氧气得电子的还原反应,燃料在负极发生失电子的反应;
D.根据电池反应:C2H5OH+3O2=2CO2+3H2O,乙醇被氧化电极反应式为C2H5OH+3H2O-12e-=2CO2+12H+,反应转移电子数为12.
解答:
解:A.在燃料电池中,燃料乙醇在负极发生失电子的反应,氧气是在正极上发生得电子的反应,则a为负极,故A错误;
B.电池工作时,电流由正极经外电路流向负极,在该电池中由b极流向a极,故B错误;
C.在燃料电池中,正极上是氧气得电子的还原反应,在酸性电解质环境下,正极的电极反应为:4H++O2+4e-=2H2O,故C错误;
D.根据电池反应:C2H5OH+3O2=2CO2+3H2O,乙醇被氧化电极反应式为C2H5OH+3H2O-12e-=2CO2+12H+,则1mol乙醇被氧化失去12mol电子,故D正确;
故选D.
B.电池工作时,电流由正极经外电路流向负极,在该电池中由b极流向a极,故B错误;
C.在燃料电池中,正极上是氧气得电子的还原反应,在酸性电解质环境下,正极的电极反应为:4H++O2+4e-=2H2O,故C错误;
D.根据电池反应:C2H5OH+3O2=2CO2+3H2O,乙醇被氧化电极反应式为C2H5OH+3H2O-12e-=2CO2+12H+,则1mol乙醇被氧化失去12mol电子,故D正确;
故选D.
点评:本题考查原电池知识,题目难度中等,本题注意把握根据电池总反应书写电极方程式的方法.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
将Na2O2投入到FeCl2溶液中,观察到的现象是( )
| A、生成白色沉淀 |
| B、生成红褐色沉淀 |
| C、没有气泡产生 |
| D、溶液变成棕黄色 |
下列说法正确的是( )
| A、利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 |
| B、水电站把机械能转化成电能,而核电站把化学能转化成电能 |
| C、在医院中,为酸中毒病人输液应采用0.9%氯化铵溶液 |
| D、棉、麻、丝、毛及合成纤维完全燃烧都只生成CO2和H2O |
下列物质既能导电又是电解质的是( )
| A、无水乙醇 | B、液氯 |
| C、硫酸铜溶液 | D、熔融的KCl |
关于原电池和电解池的电极名称,下列说法错误的是( )
| A、原电池中失去电子的一极一定为负极 |
| B、电解池中与直流电源负极相连的一极一定为阴极 |
| C、电解池中发生氧化反应的一极一定为阳极 |
| D、原电池中负极的质量一定减少 |
关于下列装置的说法正确的是( )
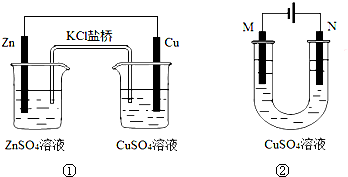

| A、装置①中盐桥内的K+移向CuSO4溶液 |
| B、装置①将电能转变为化学能 |
| C、若装置②用于铁棒镀铜,则N极为铁棒 |
| D、若装置②用于电解精炼铜,溶液中的Cu2+浓度保持不变 |
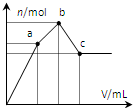 向100mL 0.1mol?L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol?L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.下列说法正确的( )
向100mL 0.1mol?L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol?L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.下列说法正确的( )| A、a点的溶液呈中性 |
| B、a点沉淀的质量比c点沉淀的质量大 |
| C、b点加入Ba(OH)2溶液的体积为250 mL |
| D、至c点完成反应,反应的离子方程式可表示为:Al3++2SO42-+NH4++2Ba2++5OH-→AlO2-+2BaSO4↓+NH3?H2O+2H2O |
下列溶液中有关微粒的物质的量浓度关系正确的是( )
| A、pH相等的下列溶液①(NH4)2SO4、②NH4HSO4、③NH4Cl,c(NH4+)的大小关系为①=③>② |
| B、0.1mol/L的NaHA溶液,若pH=4,则溶液中存在:c(HA-)>c(H+)>c(H2A)>c(A2-) |
| C、在NaHCO3和Na2CO3的混合溶液中一定存在:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
| D、在物质的量浓度之比为1:2的NaClO、NaHCO3的混合溶液中一定存在:c(HClO)+c(ClO-)=2c(HCO3-)+2c(H2CO3)+2c(CO32-) |