题目内容
如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将甲针筒内的物质压到乙针筒内,进行实验,对乙针筒里的现象所作的判断不正确的是.( )
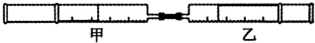

| 实验序号 | 甲针筒内物质 | 乙针筒内物质 | 乙针筒里的现象 |
| A | HCl | AgNO3溶液 | 产生白色沉淀 |
| B | NH3 | FeCl3溶液 | 出现红褐色沉淀 |
| C | CO2 | BaCl2 | 产生白色沉淀 |
| D | Cl2 | 紫色石蕊溶液 | 先变红后褪色 |
| A、A | B、B | C、C | D、D |
考点:氨的化学性质,氯气的化学性质
专题:
分析:A.盐酸与硝酸银反应生成氯化银白色沉淀;
B.氨气与水反应生成一水合氨,一水合氨与氯化铁反应生成氢氧化铁;
C.碳酸的酸性弱于盐酸;
D.氯气与水反应生成盐酸和次氯酸.
B.氨气与水反应生成一水合氨,一水合氨与氯化铁反应生成氢氧化铁;
C.碳酸的酸性弱于盐酸;
D.氯气与水反应生成盐酸和次氯酸.
解答:
解:A.盐酸与硝酸银反应生成氯化银白色沉淀,故A正确;
B.氨气与水反应生成一水合氨,一水合氨与氯化铁反应生成氢氧化铁,氢氧化铁为红褐色沉淀,故B正确;
C.碳酸的酸性弱于盐酸,二氧化碳通入氯化钡不反应,无现象,故C错误;
D.氯气与水反应生成盐酸和次氯酸,盐酸具有酸性所以石蕊先变红色,次氯酸具有漂白性,所以最后溶液褪色,故D正确;
故选:C.
B.氨气与水反应生成一水合氨,一水合氨与氯化铁反应生成氢氧化铁,氢氧化铁为红褐色沉淀,故B正确;
C.碳酸的酸性弱于盐酸,二氧化碳通入氯化钡不反应,无现象,故C错误;
D.氯气与水反应生成盐酸和次氯酸,盐酸具有酸性所以石蕊先变红色,次氯酸具有漂白性,所以最后溶液褪色,故D正确;
故选:C.
点评:本题主要考查了元素及其化合物的知识,熟悉物质的性质和发生反应的实质是解题关键,题目难度不大.

练习册系列答案
相关题目
甲醇(CH3OH)是一种有毒物质,检测甲醇含量的测试仪工作原理示意图如下.下列说法正确的是( )

| A、该装置为电能转化为化学能的装置 |
| B、a电极发生的电极反应为CH3OH-6e-+H2O═CO2↑+6H+ |
| C、当电路中有1 mol e-转移时,正极区n(H+)增加1 mol |
| D、将酸性电解质溶液改为碱性电解质溶液该测试仪不可能产生电流 |
化学与人类生产、生活、社会可持续发展密切相关.下列说法正确的是( )
| A、稀的食盐水能杀死H7N9禽流感病毒 |
| B、煤经过分馏和干馏两个物理变化,可变为清洁能源 |
| C、电镀厂的废水直接用来灌溉农田,可提高水的利用率 |
| D、用CO2合成聚碳酸酯可降解塑料,有利于减少白色污染 |
下列事实不能用平衡移动原理解释的是( )
 |  |  |  |
| A | B | C | D |
| A、A | B、B | C、C | D、D |
化学与生活息息相关,下列说法不正确的是( )
| A、干燥的Cl2和氯水均能使鲜花褪色 |
| B、Si可用于制造半导体材料 |
| C、次氯酸钠溶液是生活中常用的消毒剂 |
| D、经常食用含明矾的食品能中和过多的胃酸 |
 以氨作为燃料的固体氧化物(含有O2-燃料电池,具有全固态结构、能量效率高的特点,另外氨气含氢量高,不含碳,易液化,方便运输和贮存,是很好的氢源载体,其工作原理如图所示,下列关于直接氨固体氧化物燃料电池的说法正确的是( )
以氨作为燃料的固体氧化物(含有O2-燃料电池,具有全固态结构、能量效率高的特点,另外氨气含氢量高,不含碳,易液化,方便运输和贮存,是很好的氢源载体,其工作原理如图所示,下列关于直接氨固体氧化物燃料电池的说法正确的是( )| A、电极a为电源的阴极 |
| B、固体氧化物作为电池工作的电解质,其作用是让电子在电池内移动 |
| C、电池工作时,在a电极接触面上发生的电极反应为:2NH3+3O2--6e-=N2+3H2O |
| D、外电路的电流方向为从电极a流向电极b |
下列对化学知识的认识正确的是( )
| A、H2与T2互为同位素 |
| B、氯化铵、氯化银都属于强电解质 |
| C、离子化合物中一定不含共价键 |
| D、SO2、CO均属于酸性氧化物 |