题目内容
已知①2C(s)+O2(g)=2CO(g) △H1=-221.0kJ?mol-1 ②2H2(g)+O2(g)=2H2O(g) △H2=-483.6kJ?mol-1,则制备半水煤气的反应C(s)+H2O(g)=CO(g)+H2(g)的△H为
- A.+262.6kJ?mol-1
- B.-131.3kJ?mol-1
- C.-352.3kJ?mol-1
- D.+131.3kJ?mol-1
D
①2C(s)+O2(g) 2CO(g) ΔH1=-221.0kJ·mol-1,②2H2(g)+ O2(g)
2CO(g) ΔH1=-221.0kJ·mol-1,②2H2(g)+ O2(g) ![]() 2H2O(g) ΔH2=-483.6 kJ·mol-1,(①-②)÷2得:C(s)+H2O(g)
2H2O(g) ΔH2=-483.6 kJ·mol-1,(①-②)÷2得:C(s)+H2O(g)![]() CO(g)+H2(g),所以ΔH =(ΔH1-ΔH2)÷2=[-221.0kJ·mol-1-(-483.6kJ·mol-1)]÷2=131.3kJ·mol-1。
CO(g)+H2(g),所以ΔH =(ΔH1-ΔH2)÷2=[-221.0kJ·mol-1-(-483.6kJ·mol-1)]÷2=131.3kJ·mol-1。
①2C(s)+O2(g)
 2CO(g) ΔH1=-221.0kJ·mol-1,②2H2(g)+ O2(g)
2CO(g) ΔH1=-221.0kJ·mol-1,②2H2(g)+ O2(g) 
练习册系列答案
相关题目
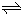
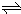 N2O4(g)△H<0,升高温度,正逆反应的速率都增大,但正反应的增速大于逆反应增速
N2O4(g)△H<0,升高温度,正逆反应的速率都增大,但正反应的增速大于逆反应增速