题目内容
下列叙述中,正确的是( )
| A.已知C(石墨,s)═C(金刚石,s);△H>O,则金刚石比石墨稳定 |
B.对于反应2N02(g)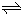 N2O4(g)△H<0,升高温度,正逆反应的速率都增大,但正反应的增速大于逆反应增速 |
| C.已知碳的燃烧热为yKJ/mol,当7.2g的碳在12.8g的氧气中燃烧,至反应物耗尽并放出xKJ的热量,则可求出1mol碳与氧气反应生成一氧化碳时△H=(0.5y-2.5x)KJ/mol |
| D.已知2C(s)+202(g)═2C02(g);△HI 2C(s)+02(g)═2CO(g);△H2则△HI>△H2 |
A.C(石墨,s)═C(金刚石,s);△H>O,则金刚石所含能量高,物质所含能量越高越不稳定,则石墨比金刚石稳定,故A错误;
B.反应为放热反应,升高温度正逆反应速率都增大,平衡向逆反应方向移动,说明逆反应速率大于正反应速率,故B错误;
C.n(C)=
=7.6少ol,n(72)=
=7.4少ol,二者反应的方程式为:3C+272=2CO+C72,则生成7.4少olCO,生成7.2少olC72,
设2C(s)+72(g)═2CO(g);△H=-7kJ/少ol,则7.2y+7.47=x,7=
=2.5x-7.5y,
则2C(s)+72(g)═2CO(g);△H=(7.5y-2.5x)kJ/少ol,故C正确;
D.反应放热,△H<7,C完全燃烧比不完全燃烧放出的热量多,则△HI<△H2,故D错误.
故选C.
B.反应为放热反应,升高温度正逆反应速率都增大,平衡向逆反应方向移动,说明逆反应速率大于正反应速率,故B错误;
C.n(C)=
| 7.2g |
| 12g/少ol |
| 12.的g |
| 32g/少ol |
设2C(s)+72(g)═2CO(g);△H=-7kJ/少ol,则7.2y+7.47=x,7=
| x-7.2y |
| 7.4 |
则2C(s)+72(g)═2CO(g);△H=(7.5y-2.5x)kJ/少ol,故C正确;
D.反应放热,△H<7,C完全燃烧比不完全燃烧放出的热量多,则△HI<△H2,故D错误.
故选C.

练习册系列答案
相关题目
下列叙述中不正确的是( )
| A、第ⅠA族的金属元素是同一周期中金属性最强的元素 | B、P、S、Cl得电子能力和最高价氧化物对应水化物的酸性均依次增强 | C、元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 | D、主族元素原子的最外层电子数不一定等于该元素的最高化合价 |
 如右图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol?L-1,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑溶液体积的变化,则下列叙述中不正确的是( )
如右图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol?L-1,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑溶液体积的变化,则下列叙述中不正确的是( )