题目内容
(1)在FeSO4溶液中,加入NaOH溶液,并放在空气中,发生反应的化学方程式是
(2)铁粉与水蒸气反应的化学方程式
(3)高炉中把铁矿石冶炼成铁是个复杂过程,主要原理是可以用CO还原Fe2O3的反应来表示,写出反应的化学方程式,并指出还原剂和氧化剂,同时标出电子的转移. .
(2)铁粉与水蒸气反应的化学方程式
(3)高炉中把铁矿石冶炼成铁是个复杂过程,主要原理是可以用CO还原Fe2O3的反应来表示,写出反应的化学方程式,并指出还原剂和氧化剂,同时标出电子的转移.
考点:化学方程式的书写,氧化还原反应,铁的化学性质,铁的氧化物和氢氧化物
专题:
分析:(1)FeSO4溶液中,加入NaOH,二者发生反应生成氢氧化亚铁,氢氧化亚铁不稳定,易被氧化生成氢氧化亚铁;
(2)铁粉和水蒸气在高温条件下发生氧化还原反应生成四氧化三铁和氢气;
(3)CO具有还原性,能将Fe2O3还原为Fe单质,该反应中C元素化合价由+2价变为+4价、Fe元素化合价由+3价变为0价,所以CO是还原剂、Fe2O3是氧化剂.
(2)铁粉和水蒸气在高温条件下发生氧化还原反应生成四氧化三铁和氢气;
(3)CO具有还原性,能将Fe2O3还原为Fe单质,该反应中C元素化合价由+2价变为+4价、Fe元素化合价由+3价变为0价,所以CO是还原剂、Fe2O3是氧化剂.
解答:
解:(1)FeSO4溶液中,加入NaOH,二者发生反应生成氢氧化亚铁,氢氧化亚铁不稳定,易被氧化生成氢氧化亚铁,反应方程式为2NaOH+FeSO4=Fe(OH)2↓+Na2SO4、4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:2NaOH+FeSO4=Fe(OH)2↓+Na2SO4、4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(2)铁粉和水蒸气在高温条件下发生氧化还原反应生成四氧化三铁和氢气,反应方程式为3Fe+4H2O(g)
Fe3O4+4H2,故答案为:3Fe+4H2O(g)
Fe3O4+4H2;
(3)CO具有还原性,能将Fe2O3还原为Fe单质,该反应中C元素化合价由+2价变为+4价、Fe元素化合价由+3价变为0价,所以CO是还原剂、Fe2O3是氧化剂,转移电子数为6,反应方程式为 ,故答案为:
,故答案为: .
.
故答案为:2NaOH+FeSO4=Fe(OH)2↓+Na2SO4、4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(2)铁粉和水蒸气在高温条件下发生氧化还原反应生成四氧化三铁和氢气,反应方程式为3Fe+4H2O(g)
| ||
| ||
(3)CO具有还原性,能将Fe2O3还原为Fe单质,该反应中C元素化合价由+2价变为+4价、Fe元素化合价由+3价变为0价,所以CO是还原剂、Fe2O3是氧化剂,转移电子数为6,反应方程式为
 ,故答案为:
,故答案为: .
.
点评:本题考查化学方程式的书写,涉及氧化还原反应,根据反应物、生成物及反应条件书写方程式即可,难点是标出电子转移方向和数目.

练习册系列答案
相关题目
分子式为CNH2NO2的羧酸和某醇酯化生成分子式为CN+2H2N+4O2的酯,反应所需羧酸和醇的质量比为1:1,则该羧酸是( )
| A、乙酸 | B、丙酸 | C、甲酸 | D、乙二酸 |
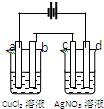 如图,以惰性电极材料为电极进行电解,在a、b、c、d各电极上析出生成物的物质的量比例关系正确的是( )
如图,以惰性电极材料为电极进行电解,在a、b、c、d各电极上析出生成物的物质的量比例关系正确的是( )| A、1:1:1:1 |
| B、2:2:1:1 |
| C、2:2:4:1 |
| D、1:2:2:4 |
设NA为阿伏加德罗常数的值,下列说法中,正确的是( )
| A、2.4 g金属镁所含电子数目为0.2 NA |
| B、1 mol H2SO4所含粒子数目为NA |
| C、17 g NH3所含中子数目为10 NA |
| D、18 g水所含分子数目为NA |
下列关于摩尔质量的论述正确的是( )
| A、氢的摩尔质量为l g/mol |
| B、1个氮分子的摩尔质量为28 g |
| C、水的摩尔质量为18 g |
| D、NO3-的摩尔质量为62 g/mol |
下列关于实验操作的说法正确的是( )
| A、学生甲认为苯酚不慎沾在皮肤上时,根据苯酚能够与65℃以上的水任意比混溶,所以最好马上用65℃以上的水进行洗涤 |
| B、学生乙在做酸碱中和滴定实验时,将标准液盐酸溶液通过移液管移入锥形瓶,并滴加1-2滴酚酞作为指示剂,而待测液氢氧化钠溶液装入碱式滴定管进行滴定 |
| C、学生丙在称量某固体样品的质量时,托盘一端放入5克砝码,并将游码用镊子沿着刻度尺向盛样品的一端移动后,停在1.2克和1.3克偏右的某一处时,天平平衡,该生马上得到该样品的质量为6.3克 |
| D、学生丁在做中和热测定时,认为应用稀的含等物质的量的H+和OH-的溶液反应来进行测定 |
碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间有如下转化关系:
根据如图转化关系推测下列说法中不正确的是( )

根据如图转化关系推测下列说法中不正确的是( )

| A、可用淀粉-KI试纸和食醋检验加碘盐中是否含有碘 |
| B、在碘水中通入Cl2,发生反应的化学方程式为5Cl2+I2+6H2O═2HIO3+10HCl |
| C、由图可知氧化性的强弱顺序为:Cl2>I2>IO3- |
| D、途径Ⅲ中若消耗1 mol Cl2,反应中转移的电子数为2NA |
 用如图表示的一些物质或概念间的从属关系中不正确的是
用如图表示的一些物质或概念间的从属关系中不正确的是
