题目内容
2.高锰酸钾是中学常用的试剂.工业上用软锰矿制备高锰酸钾流程如下.
(1)KMnO4稀溶液是一种常用的消毒剂.其消毒原理与下列物质相同的是AB(填代号).
A.84消毒液(NaClO溶液) B.双氧水 C.苯酚 D.75%酒精
(2)上述流程中可以循环使用的物质有MnO2;KOH(写化学式).
(3)理论上(若不考虑物质循环与制备过程中的损失)1mol MnO2可制得$\frac{2}{3}$ mol KMnO4.
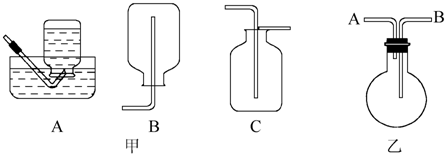
(4)该生产中需要纯净的CO2气体.写出实验室制取CO2的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑,所需气体产生装置是AC(选填代号).

分析 二氧化锰与氢氧化钾在空气中熔融,加水溶解得到K2MnO4溶液,通入二氧化碳得到KMnO4、MnO2、K2CO3,过滤除去滤渣(MnO2),滤液为KMnO4、K2CO3溶液,浓缩结晶,趁热过滤得到KMnO4晶体,滤液中含有K2CO3,在滤液中加氢氧化钙得到碳酸钙沉淀和KOH;
(1)KMnO4有强氧化性,消毒原理与84消毒液、双氧水一样;
(2)根据流程分析,最初反应物中和最终生成物中含有的物质就能循环利用;
(3)最初的原料中1mol MnO2恰好得到1mol K2MnO4,根据3K2MnO4+2CO2=2KMnO4+2K2CO3+MnO2计算;
(4)实验室用盐酸与石灰石制备二氧化碳,反应不需要加热,可以用启普发生器制备.
解答 解:二氧化锰与氢氧化钾在空气中熔融,加水溶解得到K2MnO4溶液,通入二氧化碳得到KMnO4、MnO2、K2CO3,过滤除去滤渣(MnO2),滤液为KMnO4、K2CO3溶液,浓缩结晶,趁热过滤得到KMnO4晶体,滤液中含有K2CO3,在滤液中加氢氧化钙得到碳酸钙沉淀和KOH;
(1)KMnO4有强氧化性,利用其强氧化性杀菌消毒,消毒原理与84消毒液、双氧水一样,故答案为:AB;
(2)根据流程分析可知:在开始的反应物和最终的生成物中都含有MnO2和KOH,所以二氧化锰和氢氧化钾能循环使用;
故答案为:MnO2;KOH;
(3)由2MnO2+4KOH+O2 $\frac{\underline{\;熔融\;}}{\;}$2K2MnO4+2H2O 可知最初的原料中1mol MnO2恰好得到1mol K2MnO4.由3K2MnO4+2CO2=2KMnO4+2K2CO3+MnO2知,1mol K2MnO4在反应中能得到$\frac{2}{3}$molKMnO4,
故答案为:$\frac{2}{3}$;
(4)实验室用盐酸与石灰石制备二氧化碳,其反应的方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑,反应不需要加热,可以用启普发生器制备,所以选用的装置为A或C;
故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑;AC.
点评 本题考查了物质的制备实验方案设计,涉及常见氧化剂与还原剂、氧化还原反应、化学计算和对工艺流程的理解、阅读题目获取信息的能力等,需要学生具有扎实的基础知识与灵活运用知识解决问题的能力,题目难度中等.

 教材全解字词句篇系列答案
教材全解字词句篇系列答案| A. | 前者大 | B. | 后者大 | C. | 相等 | D. | 不能确定 |
| A. | 在催化剂存在条件下苯与溴反应制溴苯 | |
| B. | 苯与浓硝酸、浓硫酸混合共热制取硝基苯 | |
| C. | 乙烯与水生成乙醇 | |
| D. | 在光照条件下甲烷和氯气反应制氯仿 |
| A. | 硬脂酸甘油酯属于高级脂肪酸甘油酯,在一定条件下可以发生水解反应 | |
| B. | 含淀粉或纤维素的物质可以制造酒精 | |
| C. | 鸡蛋清的溶液中加入硫酸铜溶液,鸡蛋清凝聚,蛋白质析出,加水稀释后又重新溶解 | |
| D. | 不同种类的氨基酸能以不同的数目和顺序彼此结合,形成更复杂的多肽化合物 |
| A. | 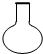 | B. | 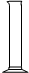 | C. |  | D. |  |
| A. | 相对原子质量 | B. | 电子层数 | C. | 核电荷数 | D. | 最外层电子数 |
| A. | 5.6g | B. | 4.4g | C. | 2.2g | D. | 1g |