题目内容
8.0℃和1.01×105 Pa条件下,13g某气体与8g CH4的分子数目相同,则该气体在相应的条件下密度为( )| A. | 0.36 g•L-1 | B. | 0.58 g•L-1 | C. | 1.16 g•L-1 | D. | 0.714 g•L-1 |
分析 根据n=$\frac{m}{M}$计算甲烷物质的量,13g某气体与8g CH4的分子数目相同,二者物质的量相等,再根据V=nVm计算气体体积,根据ρ=$\frac{m}{V}$计算气体密度.
解答 解:8g 甲烷物质的量为$\frac{8g}{16g/mol}$=0.5mol,13g某气体与8g CH4的分子数目相同,二者物质的量相等,故标况下该气体的体积为0.5mol×22.4L/mol=11.2L,故标况下该气体的密度为$\frac{13g}{11.2L}$=1.16 g•L-1,
故选:C.
点评 本题考查物质的量有关计算,可以先计算气体的摩尔质量,再根据ρ=$\frac{M}{{V}_{m}}$计算.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.下列说法正确的是( )
| A. | 化学反应不一定伴随着能量的变化 | |
| B. | 氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(g)△H=571.6kJ•mol-1 | |
| C. | 放在冰箱中的食品保质期较长,这与温度对反应速率的影响有关D.所有燃烧反应都是放热反应,所以不需吸收能量就可以进行 | |
| D. | 所有燃烧反应都是放热反应,所以不需吸收能量就可以进行 |
16.下列说法正确的是( )
| A. | 某次酸雨的pH为4.3,是由于溶解了CO2 | |
| B. | 生铁、不锈钢、青铜都属于合金 | |
| C. | 汽车尾气不会引起呼吸道疾病 | |
| D. | 普通玻璃的主要成分是纯碱、石灰石和石英 |
13.用下列方法都可以产生氧气:①加热高锰酸钾;②向过氧化钠中通入二氧化碳;③向H2O2溶液中加入二氧化锰;④加热氯酸钾与二氧化锰的混合物.若要得到质量相同的氧气,反应过程中电子转移的数目之比为( )
| A. | 1:1:1:1 | B. | 2:1:1:2 | C. | 1:2:1:2 | D. | 1:2:2:1 |
17.缺乏下列哪种元素可导制贫血( )
| A. | 硫 | B. | 磷 | C. | 铁 | D. | 锌 |
18.在25mL碱式滴定管中盛放KOH溶液,将溶液的凹面调至“0”刻度后,再把其中的液体全部放出,则流出液体体积( )
| A. | 25mL | B. | 大于25mL | C. | 小于25mL | D. | 都不正确 |
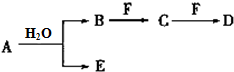 A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题:
A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题: ;D中所含化学键的类型离子键、共价键.
;D中所含化学键的类型离子键、共价键.