题目内容
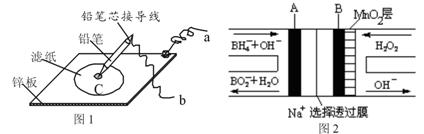
NaBH4/H2O2燃料电池(DBFC)的结构如下图,有关该电池的说法正确的是

- A.电极B是燃料电池的负极
- B.电池的电极A反应为:BH4-+8OH--8e-===BO2-+6H2O
- C.放电过程中,Na+从正极区向负极区迁移
- D.在电池反应中每消耗1 L 6 mol/L H2O2溶液,理论上流过电路中的电子为6NA个
B
在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。NaBH4在反应中失去电子,所以A是负极。双氧水得电子,因此B是正极。所以AC不正确,B正确。1mol双氧水在反应中得到2mol电子,所以D中应该转移12电子,不正确。答案选B。
在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。NaBH4在反应中失去电子,所以A是负极。双氧水得电子,因此B是正极。所以AC不正确,B正确。1mol双氧水在反应中得到2mol电子,所以D中应该转移12电子,不正确。答案选B。

练习册系列答案
 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案
相关题目
图1是在金属锌板上贴上一张用某溶液浸湿的滤纸,图2是NaBH4/H2O2燃料二次电池,则下列说法正确的是( )


| A、图1若用硫酸钠和酚酞的混合溶液浸湿滤纸,用导线将a、b直接相连,则铅笔芯C点反应为O2+2H2O+4e-?4OH- | B、图2放电过程中,Na+从正极区向负极区迁移 | C、图2充电时阳极区反应为BH-4-8e-+8OH-?BO-2+6H2O | D、图1若用KI淀粉溶液浸湿滤纸,用导线将a、b与A、B电极相连,若铅笔芯C点处出现蓝色,则b接的是A电极 |
 NaBH4/H2O2燃料电池(DBFC)的结构如图,有关该电池的说法正确的是( )
NaBH4/H2O2燃料电池(DBFC)的结构如图,有关该电池的说法正确的是( ) (2011?南京二模)三效催化转化器可减少汽车尾气中的主要污染物(CO、NOx等),部分反应如下:
(2011?南京二模)三效催化转化器可减少汽车尾气中的主要污染物(CO、NOx等),部分反应如下: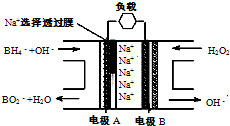 (2010?启东市模拟)直接NaBH4/H2O2燃料电池(DBFC)的结构如图,“负极材料采用Pt/C,正极材料采用MnO2”,有关该电池的说法正确的是
(2010?启东市模拟)直接NaBH4/H2O2燃料电池(DBFC)的结构如图,“负极材料采用Pt/C,正极材料采用MnO2”,有关该电池的说法正确的是