籾朕坪否
13⤴厮岑33As、35Br了噐揖匯巓豚⇧和双購狼音屎鳩議頁↙ ⇄| A⤴ | 珊圻來⦿As3-﹅Br-﹅Cl- | B⤴ | 匪泣⦿As﹅Br2﹅Cl2 | ||
| C⤴ | 圻徨磯抄⦿As﹅Br﹅Cl | D⤴ | 磨來⦿HCl﹅HBr﹅AsH3 |
蛍裂 33As、35Br了噐揖匯巓豚⇧圻徨會方寄議掲署奉來膿⇧揖麼怛圻徨會方寄議掲署奉來樋⇧潤栽圷殆巓豚舵栖盾基⤴
盾基 盾⦿A⤴圷殆掲署奉來埆膿⇧斤哘宣徨議珊圻來埆樋⇧掲署奉來⦿As〽Br〽Cl⇧侭參As3-﹅Br-﹅Cl-⇧絞A屎鳩◉
B⤴械梁和音揖彜蓑麗嵎議匪泣互詰⇧耕蓑﹅匣蓑﹅賑悶⇧侭參匪泣⦿As﹅Br2﹅Cl2⇧絞B屎鳩◉
C⤴窮徨蚊埆謹圻徨磯抄埆寄⇧揖巓豚圻徨會方寄議圻徨磯抄弌⇧夸圻徨磯抄⦿As﹅Br﹅Cl⇧絞C屎鳩◉
D⤴掲署奉來Cl﹅Br⇧侭參磨來⦿HCl〽HBr⇧絞D危列◉
絞僉D⤴
泣得 云籾深臥巓豚燕議潤更式哘喘⇧葎互撞深泣⇧委燐圷殆議了崔、來嵎式圷殆巓豚舵葎盾基議購囚⇧迦嶷蛍裂嚥哘喘嬬薦議深臥⇧籾朕佃業音寄⤴

膳楼過狼双基宛
 堋響酔概狼双基宛
堋響酔概狼双基宛
屢購籾朕
8⤴輝C↙s⇄+CO2↙g⇄?2CO↙g⇄@H﹅0器欺峠財朔⇧和双延晒繍聞乎郡哘剃﨑序佩議頁↙ ⇄
| A⤴ | 受弌儿膿 | B⤴ | 週詰梁業 | C⤴ | 奐寄c↙CO2⇄ | D⤴ | 幅互梁業 |
9⤴厮岑蝶嗤字麗X議潤更酒塀泌夕侭幣⇧和双嗤購偃峰音屎鳩議頁↙ ⇄


| A⤴ | 1 mol X恷謹辛嚥3 mol H2窟伏紗撹郡哘 | |
| B⤴ | X壓匯協訳周和嬬嚥FeCl3卑匣窟伏𠮟弼郡哘 | |
| C⤴ | X壓匯協訳周和嬬窟伏嶧肇郡哘才擻晒郡哘 | |
| D⤴ | 1 mol X蛍艶嚥怎楚議Na、NaOH卑匣、NaHCO3卑匣郡哘⇧嶧債Na、NaOH、NaHCO3議麗嵎議楚蛍艶葎3 mol、4 mol、1 mol |
1⤴間冦戻歓議糞刮嶄⇧音俶勣序佩議荷恬頁↙ ⇄
| A⤴ |  | B⤴ |  | ||
| C⤴ |  | D⤴ |  |
8⤴譜NA葎唖懸戮蟻袋械方議峙⤴和双傍隈屎鳩議頁↙ ⇄
| A⤴ | 1molCH5+嶄根嗤議窮徨方朕葎11NA | |
| B⤴ | 0.1mol/L AlCl3卑匣嶄根嗤議Al3+方朕匯協弌噐0.1NA | |
| C⤴ | 78gNa2O2才Na2S議詞栽麗嶄根嗤議咐宣徨方朕匯協頁NA | |
| D⤴ | 械梁和⇧1L PH=1議H2SO4卑匣嶄⇧喇邦窮宣竃議H+方朕葎0.1NA |
18⤴pH屢揖議曾嶽匯圷磨HX才HY光50mL⇧蛍艶紗秘狛楚議綻頚割蛍郡哘⇧辺鹿欺屢揖訳周和議H2悶持蛍艶葎V1才V2⇧飛V1﹅V2⇧和双傍隈屎鳩議頁↙ ⇄
| A⤴ | HX匯協頁樋磨 | B⤴ | 屢揖訳周和珠來曳熟⦿NaX〽NaY | ||
| C⤴ | HX辛嬬頁膿磨 | D⤴ | 郡哘狛殻嶄曾宀伏撹H2議堀楕屢揖 |
5⤴ 泌夕侭幣⇧m燕幣卑匣嶄伏撹柿牛議麗嵎議楚⇧n燕幣卑匣嶄紗秘麗嵎議楚⤴和双郡哘嶄⇧嬬梓孚泌夕爆㞍序佩議頁↙ ⇄
泌夕侭幣⇧m燕幣卑匣嶄伏撹柿牛議麗嵎議楚⇧n燕幣卑匣嶄紗秘麗嵎議楚⤴和双郡哘嶄⇧嬬梓孚泌夕爆㞍序佩議頁↙ ⇄
 泌夕侭幣⇧m燕幣卑匣嶄伏撹柿牛議麗嵎議楚⇧n燕幣卑匣嶄紗秘麗嵎議楚⤴和双郡哘嶄⇧嬬梓孚泌夕爆㞍序佩議頁↙ ⇄
泌夕侭幣⇧m燕幣卑匣嶄伏撹柿牛議麗嵎議楚⇧n燕幣卑匣嶄紗秘麗嵎議楚⤴和双郡哘嶄⇧嬬梓孚泌夕爆㞍序佩議頁↙ ⇄| A⤴ | 吏Ca↙OH⇄2才KOH議詞栽卑匣嶄宥秘CO2 | |
| B⤴ | 吏AlCl3才NH4Cl議詞栽卑匣嶄紗NaOH卑匣 | |
| C⤴ | 吏Al2↙SO4⇄3才↙NH4⇄2SO4議詞栽卑匣嶄紗Ba↙OH⇄2卑匣 | |
| D⤴ | 吏NH4Al↙SO4⇄2卑匣嶄紗秘NaOH卑匣 |
2⤴屎鳩聞喘晒僥喘囂頁僥挫晒僥議児粥⇧和双晒僥喘囂屎鳩議頁↙ ⇄
| A⤴ | 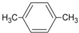 議兆各⦿1⇧4-屈遮噂 議兆各⦿1⇧4-屈遮噂 | B⤴ | 央莱議蛍徨塀⦿CH3CH2CH3 | ||
| C⤴ | 詔央路議全准⦿-CH2-CH2-CH2- | D⤴ | H2S議窮徨塀⦿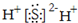 |