题目内容
下列有关实验现象和解释或结论都正确的是
选项 实验操作 现象 解释或结论
A 把SO2通入紫色石蕊试液中 紫色褪去 SO2具有漂白性
B 把浓硫酸滴到pH试纸上 试纸变红 浓硫酸具有酸性
C 将充满NO2的密闭玻璃球浸泡在热水中 红棕色变浅 反应2NO2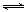 N2O4的△H<0
N2O4的△H<0
D 向AgCl沉淀中滴加KI溶液 白色沉淀变为黄色 溶度积:AgI比AgCl更小
D
【解析】
试题分析:二氧化硫是酸性氧化物,易溶于水,与水反应生成亚硫酸,则二氧化硫气体能使紫色石蕊试液变红,但是不能褪色,证明二氧化硫具有酸性氧化物的性质,故A错误;浓硫酸具有酸性、脱水性,能使pH试纸先变红后变黑,因为它能使纤维素脱水炭化,证明它具有酸性和脱水性,故B错误;红棕色的二氧化氮气体变为无色的四氧化二氮气体是放热反应,升高温度平衡向吸热反应方向移动,则玻璃球内气体红棕色变深,而不是变浅,故C错误;溶解度小的沉淀转化为溶解度更小的沉淀容易实现,白色的氯化银沉淀变为黄色的碘化银沉淀,说明溶解度:AgI<AgCl,故D正确。
考点:考查化学实验方案的设计与评价,涉及元素化合物的主要性质、温度对化学平衡的影响、沉淀的转化规律等。

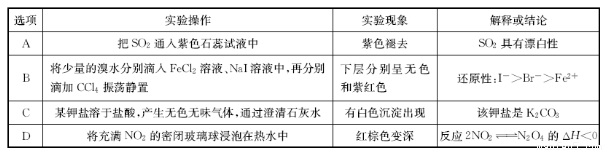
| A、把二氧化硫通入紫色石蕊试液中,紫色褪去,说明二氧化硫具有漂白性 | B、将少量的溴水分别滴入FeCl2溶液、NaI溶液中,再分别滴加CCl4振荡静置,下层分别呈无色和紫红色,说明还原性:I->Br->Fe2+ | C、某钾盐溶于盐酸,产生无色无味气体,通过澄清石灰水,有白色沉淀出现,说明该钾盐是K2CO3 | D、将充满二氧化氮的密闭玻璃球浸泡在热水中,红棕色变深,说明反应2NO2?N2O4的△H<0 |