题目内容
(16分)某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,实验小组利用A制备Al(OH)3的操作流程如下:

据此回答下列问题:
(1)I、II、III、IV四步中分离溶液和沉淀所采取的操作名称是 ,该实验操作所用到的玻璃仪器有 。
(2)根据上述流程,写出D、E所含物质的化学式:
沉淀D ;溶液E 、 。
(3)写出②、③反应的离子方程式:
② ;③ ;
(1)过滤 (2分) 玻璃棒、烧杯、漏斗(全对给3分,少一个减1分)
(2)Fe2O3 (2分) (NH4)2SO4 K2SO4(全对给3分,少一个减2分)
(3)② Al3++3NH3·H2O==Al(OH)3↓+3NH4+(3分)
③AlO2—+ CO2+2H2O== Al(OH)3↓+ HCO3-(3分)
【解析】
试题分析: Al2O3和Fe2O3不溶于水,则沉淀C为Al2O3和Fe2O3,氧化铁与碱不反应,则沉淀D为Fe2O3,反应②③中生成的沉淀为Al(OH)3,受热分解生成Al2O3,反应②为KAl(SO4)2、氨水的反应,则溶液E为K2SO4、(NH4)2SO4,(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离方法为过滤;(2)由上述分析可知, D为Fe2O3,E为K2SO4、(NH4)2SO4;(3)反应②为Al3++3NH3.H2O=Al(OH)3↓+3NH4+,反应③为AlO2—+ CO2+2H2O== Al(OH)3↓+ HCO3-。
考点:考查镁铝的重要化合物。

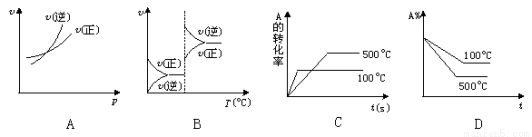
 2C(g) ΔH﹥0,下列图象中正确的是
2C(g) ΔH﹥0,下列图象中正确的是