题目内容
下列离子方程式,不正确的是
A.用氨水吸收少量二氧化硫: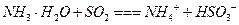 |
B.100 mL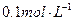 的 的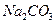 溶液中加入0.01 mol 溶液中加入0.01 mol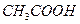 : :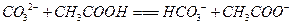 |
C.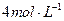 的 的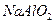 溶液和 溶液和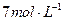 的盐酸等体积均匀混合: 的盐酸等体积均匀混合: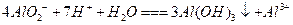 |
D.在含有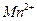 的溶液中加入 的溶液中加入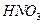 再加入 再加入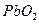 ,则反应体系显紫红色: ,则反应体系显紫红色: |
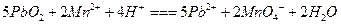
A
解析

练习册系列答案
相关题目
题目内容
下列离子方程式,不正确的是
A.用氨水吸收少量二氧化硫: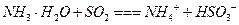 |
B.100 mL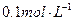 的 的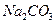 溶液中加入0.01 mol 溶液中加入0.01 mol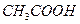 : :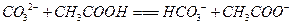 |
C.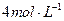 的 的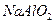 溶液和 溶液和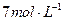 的盐酸等体积均匀混合: 的盐酸等体积均匀混合: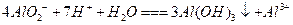 |
D.在含有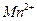 的溶液中加入 的溶液中加入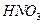 再加入 再加入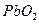 ,则反应体系显紫红色: ,则反应体系显紫红色: |
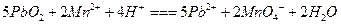
A
解析
