题目内容
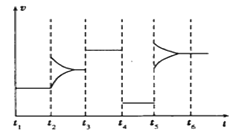
【题目】某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应:![]() ,达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的关系如图所示。请回答下列问题:
,达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的关系如图所示。请回答下列问题:

![]() 反应方程式中的
反应方程式中的![]() _______,30min时改变的反应条件是_______。
_______,30min时改变的反应条件是_______。
![]() 时反应的平衡常数_______
时反应的平衡常数_______![]() 时反应的平衡常数
时反应的平衡常数![]() 填:
填:![]() 、
、![]() 或
或![]() 。
。
![]() 该反应的正反应为________
该反应的正反应为________![]() 填:“放热”或“吸热”
填:“放热”或“吸热”![]() 反应。
反应。
![]() 反应过程中B的转化率最大的时间段是____________。
反应过程中B的转化率最大的时间段是____________。
【答案】1 扩大容器体积![]() 或减小压强
或减小压强![]() = 放热
= 放热 ![]()
【解析】
![]() 由图像可知,30min时,A和C的浓度成比例减小,则改变条件为扩大容器体积
由图像可知,30min时,A和C的浓度成比例减小,则改变条件为扩大容器体积![]() 或减小压强
或减小压强![]() ,平衡不发生移动,则两边系数相等;
,平衡不发生移动,则两边系数相等;
![]() 时和
时和![]() 时温度相同,则平衡常数相等;
时温度相同,则平衡常数相等;
![]() 时,A、C浓度不变,正逆反应速率瞬时变大,且平衡逆向移动;
时,A、C浓度不变,正逆反应速率瞬时变大,且平衡逆向移动;
![]() 时建立平衡,
时建立平衡,![]() 平衡不移动,40min后平衡左移。
平衡不移动,40min后平衡左移。
![]() 由图像可知,30min时,A和C的浓度成比例减小,则改变条件为扩大容器体积
由图像可知,30min时,A和C的浓度成比例减小,则改变条件为扩大容器体积![]() 或减小压强
或减小压强![]() ,平衡不发生移动,则两边系数相等,故
,平衡不发生移动,则两边系数相等,故![]() ,故答案为:1;扩大容器的体积
,故答案为:1;扩大容器的体积![]() 或减小压强
或减小压强![]() ;
;
![]() 时和
时和![]() 时温度相同,则平衡常数相等,故答案为:
时温度相同,则平衡常数相等,故答案为:![]() ;
;
![]() 时,A、C浓度不变,正逆反应速率瞬时变大,且平衡逆向移动,故40min时改变的条件是温度升高,平衡左移,则正反应放热,故答案为:放热;
时,A、C浓度不变,正逆反应速率瞬时变大,且平衡逆向移动,故40min时改变的条件是温度升高,平衡左移,则正反应放热,故答案为:放热;
![]() 时建立平衡,
时建立平衡,![]() 平衡不移动,40min后平衡左移,则B的转化率最大的时间段是
平衡不移动,40min后平衡左移,则B的转化率最大的时间段是![]() ,故答案为:
,故答案为:![]() 。
。

 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案【题目】某化学活动小组设计如图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的固体物质。
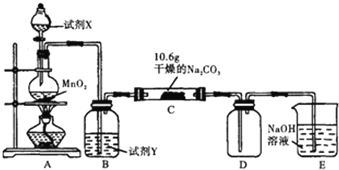
(1)装置A中发生反应的化学方程式是___。
(2)试剂Y是___;作用是___。
(3)已知:通入一定量的氯气后,测得D中有一种常温下为黄红色的气体,其为含氯的氧化物.可以确定的是C中含有氯元素的盐只有一种,且含有NaHCO3,现对C中反应后固体的成分进行猜想和探究。
提出合理假设。
假设1:存在两种成分:NaHCO3和物质W;
假设2:存在三种成分:NaHCO3、Na2CO3和物质W。
则上述假设中物质W为___(填化学式)。
设计方案,进行实验。请填写相应的实验步骤以及预期现象和结论。
限选实验试剂:稀H2SO4、稀HNO3、BaCl2溶液、Ba(OH)2溶液、AgNO3溶液。
实验步骤 | 预期现象和结论 |
步骤1:取C中的少量固体样品于试管中,滴加足量蒸馏水至固体溶解,然后将所得溶液分别置于A、B试管中 | |
步骤2:向A试管中滴加___ | ①若无明显现象,证明固体中不含___ ②若出现___(填现象和结论) |
步骤3:向B试管中滴加___ | 若溶液中出现白色沉淀,则证明含有氯元素的盐;结合步骤2中①,则假设1成立;结合步骤2中②,则假设2成立 |
(4)若假设1成立,已知C中有0.1molCl2参加反应,推知C中反应的化学方程式为___。
【题目】请根据要求填写下列空白:
(1)NaHCO3溶液呈碱性的原因是 ______________(用方程式和必要文字表示),写出该溶液存在的物料守恒的关系式 ________________。
(2)把AlCl3溶液蒸干、灼烧,最后得到的主要产物是________________________。
(3)若想除去CuCl2 溶液中混有FeCl3杂质,则往往加入试剂 ______________。
①NaOH ②NH3·H2O ③CuO ④CuCO3
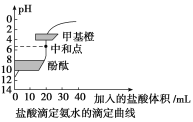
(4)在酸碱滴定中,我们用0.1000mol/L HCl来滴定未知浓度的NaOH溶液,①在滴定过程中,操作或说法错误的是_______________。
a.滴定终点为:当滴完最后一滴恰好变色,且在半分钟内不恢复原色
b.进行中和滴定操作时,左手震荡锥形瓶,右手转动活塞控制液滴流速,眼睛要始终注视滴定管内溶液液面的变化
c.酸式滴定管中的盐酸装液前未经润洗,导致所测定的c(NaOH)偏低。
d.酸式滴定管在滴定前有气泡,滴定后气泡消失,导致所测定的c(NaOH)偏高
②某学生根据三次实验分别记录有关数据如下:
滴定次数 | 待测氢氧化钠 溶液的体积/mL | 0.1000mol/L盐酸的体积(mL) | ||
滴定前刻度 | 滴定后刻度 | 溶液体/mL | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
请选用其中合理的数据列式计算该氢氧化钠溶液的物质的量浓度:c(NaOH)=________________