题目内容
NA代表阿伏加德罗常数,下列说法正确的是
- A.NA个Na变成Na+时失去的电子数目为11NA
- B.1molH2和1molH2O所含分子数相等,但在相同状况下,所占体积一定不相等
- C.质量相等的不同的纯净物,物质的量越多,则其摩尔质量越小
- D.标准状况下,22.4L氧气和臭氧的混合物中所含氧原子数为2.5NA
C
分析:A、1个钠原子失去1个电子形成1个钠离子,根据n=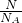 计算钠物质的量,在根据N=nNA计算失去电子数;
计算钠物质的量,在根据N=nNA计算失去电子数;
B、通常情况下,水是液体,氢气是气体,体积不相等;
C、根据摩尔质量的定义判断;
D、氧气和臭氧的物质的量之比不一定是1:1,无法计算.
解答:A、NA个Na的物质的量为1mol,变成Na+时失去的电子数目为NA,故A错误;
B、通常情况下,水是液体,氢气是气体,体积不相等;若水在一定条件为气态时,相同条件,1molH2和1molH2O,所占体积相等,故B错误;
C、摩尔质量M=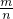 ,质量相等,物质的量越大,M值越小,故其摩尔质量越小,故C正确;
,质量相等,物质的量越大,M值越小,故其摩尔质量越小,故C正确;
D、氧气为双原子分子,臭氧是3原子分子,标准状况下,22.4L氧气和臭氧的混合物的物质的量为1mol,所以2mol<n(O)<3mol,氧气和臭氧的物质的量之比无法知道,无法计算氧原子数目,故D错误.
故选C.
点评:本题考查常用化学计量有关计算,难度不大,旨在考查学生对基础知识的掌握.
分析:A、1个钠原子失去1个电子形成1个钠离子,根据n=
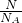 计算钠物质的量,在根据N=nNA计算失去电子数;
计算钠物质的量,在根据N=nNA计算失去电子数;B、通常情况下,水是液体,氢气是气体,体积不相等;
C、根据摩尔质量的定义判断;
D、氧气和臭氧的物质的量之比不一定是1:1,无法计算.
解答:A、NA个Na的物质的量为1mol,变成Na+时失去的电子数目为NA,故A错误;
B、通常情况下,水是液体,氢气是气体,体积不相等;若水在一定条件为气态时,相同条件,1molH2和1molH2O,所占体积相等,故B错误;
C、摩尔质量M=
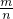 ,质量相等,物质的量越大,M值越小,故其摩尔质量越小,故C正确;
,质量相等,物质的量越大,M值越小,故其摩尔质量越小,故C正确;D、氧气为双原子分子,臭氧是3原子分子,标准状况下,22.4L氧气和臭氧的混合物的物质的量为1mol,所以2mol<n(O)<3mol,氧气和臭氧的物质的量之比无法知道,无法计算氧原子数目,故D错误.
故选C.
点评:本题考查常用化学计量有关计算,难度不大,旨在考查学生对基础知识的掌握.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目