题目内容
【题目】如图甲为锌铜原电池装置,乙为电解熔融氯化钠装置。则下列说法正确的是( )
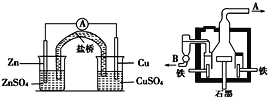
图甲 图乙
A.乙装置中B是氯气出口,A是钠出口
B.乙装置中铁极的电极反应式为:2Na-2e-=2Na+
C.甲装置中锌为负极发生还原反应,铜为正极,发生氧化反应
D.甲装置盐桥可以使反应过程中溶液保持电中性
【答案】D
【解析】
A、氯离子在阳极上转化为氯气,则A是氯气出口,Na+在阴极上得电子生成Na,则B是钠出口,选项A错误;
B、电解熔融氯化钠时应该用惰性电极作阳极,如果Fe作阳极,则Fe在阳极失电子,所以C为阳极,电极反应式为:2Cl--2e-═Cl2↑,选项B错误;
C、原电池中,活泼性强的作负极,所以甲装置中锌为负极,失电子发生氧化反应,活泼性较弱的作正极,铜为正极,发生还原反应,选项C错误;
D、盐桥的作用是形成闭合回路,并使两边溶液保持电中性,阳离子移向右池,阴离子移向左池,选项D正确;
答案选D。

练习册系列答案
相关题目