题目内容
要除去苯中的苯酚杂质,通常采用的方法是( )
| A、加水振荡后用分液漏斗分离 |
| B、加稀盐酸振荡后用分液漏斗分离 |
| C、加氢氧化钠溶后用分液漏斗分离 |
| D、加溴水振荡后滤去白色沉淀 |
考点:物质的分离、提纯的基本方法选择与应用
专题:化学实验基本操作
分析:苯酚与NaOH反应,而苯不能,加NaOH溶液后分层,以此解答.
解答:
解:A.加水后苯酚溶于苯,不能利用分液漏斗分离,故A错误;
B.二者与盐酸都不反应,不能用于分离,故B错误;
C.加NaOH溶液振荡后,苯酚反应与苯分层,则静置分液可除杂,故C正确;
D.加入溴水,苯酚和溴反应生成的三溴苯酚溶于苯,不能得到纯净的苯,故D错误.
故选C.
B.二者与盐酸都不反应,不能用于分离,故B错误;
C.加NaOH溶液振荡后,苯酚反应与苯分层,则静置分液可除杂,故C正确;
D.加入溴水,苯酚和溴反应生成的三溴苯酚溶于苯,不能得到纯净的苯,故D错误.
故选C.
点评:本题考查物质的分离、提纯,为高频考点,注意把握相关物质的性质的异同,把握操作方法和注意事项,学习中注意相关基础知识的积累,题目难度不大.

练习册系列答案
相关题目
以下是一些常用危险化学品的标志,其中装运浓硫酸的包装箱应贴的图标是( )

| A、图中所示标志是腐蚀品标志 |
| B、图中所示标志是易燃品标志 |
| C、图中所示标志是爆炸品标志 |
| D、图中所示标志是剧毒品标志 |
要从BaCl2、NaCl的混和溶液中分别得到纯净的BaCl2和 NaCl晶体,在一系列的操作中应选用的试剂是( )
| A、K2CO3、稀盐酸 |
| B、Na2CO3、稀盐酸 |
| C、Na2CO3、稀硫酸 |
| D、NaOH、稀盐酸 |
下列属于酸性食物的是( )
| A、苹果 | B、西瓜 | C、梨 | D、鸡肉 |
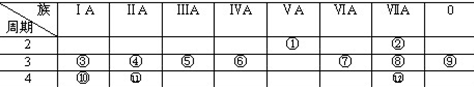
 已知A、B、C、D、E都是元素周期表中的前四周期元素,它们原子序数的大小关系为A<C<B<D<E.又知A原子的p轨道为半充满,其形成的简单氢化物的沸点是同主族非金属元素的氢化物中最高的.D原子得到一个电子后其3p轨道将全充满.B+离子比D原子形成的离子少一个电子层.C与B可形成BC型的离子化合物.E的原子序数为29.
已知A、B、C、D、E都是元素周期表中的前四周期元素,它们原子序数的大小关系为A<C<B<D<E.又知A原子的p轨道为半充满,其形成的简单氢化物的沸点是同主族非金属元素的氢化物中最高的.D原子得到一个电子后其3p轨道将全充满.B+离子比D原子形成的离子少一个电子层.C与B可形成BC型的离子化合物.E的原子序数为29.