题目内容
18.某仅由碳、氢两种元素组成的有机化合物,经测定其相对分子质量为58.取该有机物样吕11.6g,在纯氧中完全燃烧,将产物先后通过足量的浓硫酸和碱石灰,两者分别增重18g和35.2g.试求有机物的分式,并写出其可能的结构简式.分析 根据有机物的质量和相对分子质量可计算有机物的物质的量,根据生成的水和二氧化碳的质量可计算有机物中含有的C、H原子个数,结合相对分子质量可计算O原子个数,进而可求得分子式,并以此确定可能的结构简式.
解答 解:浓硫酸增重的是水的质量,故n(H2O)=$\frac{18g}{18g/mol}$=1mol,其中含有的n(H)=2mol
碱石灰增重的质量为二氧化碳的质量,故n(CO2)=$\frac{35.2g}{44g/mol}$=0.8mol,其中含有的n(C)=0.8mol
故N(C):N(H)=0.8mol:2mol=2:5
故此反应物最简式为C2H5,设此有机物的分子式为(C2H5)n,
又因为有机物分子量为58,
故有29n=58,解得n=2.
故此有机物的分子式为C4H10.即为丁烷.
根据碳链异构可知,可能的结构简式有CH3CH2CH2CH3、CH3CH(CH3)CH3.
答:该有机化合物分子式为C4H10,可能的结构简式有CH3CH2CH2CH3、CH3CH(CH3)CH3.
点评 本题考查有机物分子式的确定,侧重于学生分析能力和计算能力的考查,题目难度不大,注意根据相对分子质量确定氧原子个数.

练习册系列答案
相关题目
8.某工业生产经过以下转化步骤:
下列说法中不正确的是( )

下列说法中不正确的是( )
| A. | 该过程是一种新的硫酸生产方法 | |
| B. | C2H5OSO3H具有酸性 | |
| C. | 该过程中①、②是加成反应 | |
| D. | 该过程中③、④可看做酯类的水解反应 |
9.我国最早使用的合金是( )
| A. | 青铜 | B. | 低碳钢 | C. | 铝合金 | D. | 黄铜 |
6.如图所示,△H1=-393.5kJ•mol-1,△H2=-395.4kJ•mol-1,下列说法正确的是( )
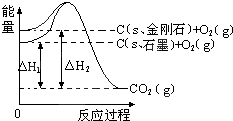

| A. | 1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ | |
| B. | 石墨和金刚石的转化是物理变化 | |
| C. | 金刚石的稳定性强于石墨 | |
| D. | C(s、石墨)═C(s、金刚石)△H=+1.9 kJ•mol-1 |
13.在集气瓶中的甲烷和氯气的混合气体光照一段时间后,移开玻璃片,在实验的过程中可能观察到的现象是( )
| A. | 集气瓶中气体的颜色不变 | B. | 集气瓶中有火星出现 | ||
| C. | 集气瓶内壁上有油状液体出现 | D. | 集气瓶口有棕黄色烟出现 |
3.在空气吹出法的工艺中,有选用纯碱溶液作溴蒸气吸收剂的,也有选用SO2作溴蒸气吸收剂的,下列有关说法正确的是( )
| A. | 两种吸收过程中,Br2只作氧化剂 | |
| B. | 两种吸收过程都发生了氧化还原反应 | |
| C. | 用纯碱溶液作吸收剂时,纯碱作还原剂 | |
| D. | 用纯碱溶液作吸收剂只发生了复分解反应 |
