题目内容
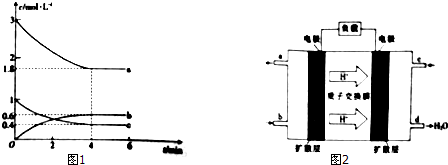
7.甲醇是一种低碳能源,在全球能源危机和环境污染的背景下具有良好的发展前景,在催化剂作用下可用H2和CO合成甲醇,反应的化学方程式为2H2(g)+CO(g)$\stackrel{催化剂}{?}$CH3OH(g),三种物质的物质的量浓度随时间变化的关系如图1所示.试回答下列问题:(1)代表H2浓度变化的曲线为a(填“a”“b”或“c”).
(2)提出一条可以加快反应速率的措施:加压或者升温.
(3)0-4 min内,CH3OH的平均反应速率为:0.15mol/(L•min).
(4)我国某高校化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆.甲醇燃料电池的工作原理如图2所示.
①该电池工作时,c口通入的物质为O2.
②该电极正极上的电极反应式为O2+4e-+4H+=2H2O.
分析 (1)根据2H2(g)+CO(g)$\stackrel{催化剂}{?}$CH3OH反应,H2浓度变化在减小并且是CO的2倍判断;
(2)可以加快反应速率的措施为加压或者升温等;
(3)根据CH3OH的平均反应速率=$\frac{△c}{△t}$计算;
(4)在甲醇燃料电池中,燃料甲醇作负极,发生失电子的氧化反应,氧气作正极,发生得电子的还原反应.
解答 解:(1)由2H2(g)+CO(g)$\stackrel{催化剂}{?}$CH3OH反应,H2浓度变化在减小并且是CO的2倍,所以代表H2浓度变化的曲线为a,故答案为:a;
(2)可以加快反应速率的措施为加压或者升温,故答案为:加压或者升温;
(3)根据图象CH3OH为生成物,即代表CH3OH浓度变化的曲线为b,则0-4 min内,CH3OH的平均反应速率=$\frac{△c}{△t}$=$\frac{0.6mol/L}{4min}$=0.15mol/(L•min),故答案为:0.15mol/(L•min);
(4)①在甲醇燃料电池中,燃料甲醇作负极,氧气作正极,电解质中的阳离子移向正极,所以c口通入的物质为氧气,故答案为:O2;
②正极上为氧气得电子发生还原反应,电极反应式为O2+4e-+4H+=2H2O,故答案为:O2+4e-+4H+=2H2O.
点评 本题是一道关于化学平衡图象的分析与反应速率的计算以及燃料电池的工作原理知识的考题,要求学生具有分析和解决问题的能力,难度不大.

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
17.分子式为C8H16O2的有机物A,它能在酸性条件下水解生成B和C,且B在一定条件下能转化成C.则有机物A的可能结构有( )
| A. | 1种 | B. | 2种 | C. | 4种 | D. | 8种 |
15.下列说法正确的是( )
| A. | 苯酚和苯甲醇互为同系物 | |
| B. | 塑料、合成纤维、涂料被称为“三大合成材料” | |
| C. | 天然油脂的主要成分是高级脂肪酸 | |
| D. | 淀粉和纤维素水解的最终产物都是葡萄糖 |
2.下列有关化学用语表示正确的是( )
| A. | 乙烯的比例模型: | |
| B. | 甲基的电子式: | |
| C. | 乙醇的分子式C2H6O | |
| D. | 中子数为53、质子数为78的碘原子:${\;}_{53}^{131}$I |
12.次氯酸可用于杀菌消毒.已知25°C时:[①HClO(aq)+OH-(aq)=ClO-(aq)+H2O(l)△H=-Q1kJ•mol-1②H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ•mol-1下列说法正确的是( )
| A. | 已知酸性H2SO3>HClO>HSO3-,则向Na2SO3溶液中加入HClO的离子方程式为:SO32-+HClO=HSO3-+ClO- | |
| B. | 将20ml 1mol/L HClO溶液与10ml 1mol/L NaOH溶液混合后,所得的混合溶液中一定存在:2c(H+)-2c(OH-)=c(ClO-)-c(HClO) | |
| C. | 在25°C时,次氯酸的电离方程式及热效应可表示为:HClO(aq)?H+(aq)+ClO-(aq)△H=-(57.3+Q1)kJ•mol-1 | |
| D. | 已知酸性CH3COOH>HClO,则等浓度CH3COONa和NaClO的混合液中:c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+) |




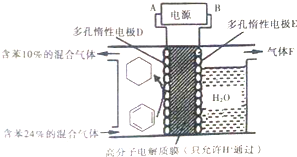 氢气是一种理想的“绿色能源”,利用氢能需选择合适的储氢材料.目前正在研究和使用的储氢材料有镁系合金、稀土系合金等.
氢气是一种理想的“绿色能源”,利用氢能需选择合适的储氢材料.目前正在研究和使用的储氢材料有镁系合金、稀土系合金等. (g)$?_{高温}^{FeSO_{4}/Al_{2}O_{3}}$
(g)$?_{高温}^{FeSO_{4}/Al_{2}O_{3}}$ (g)+3H2(g)
(g)+3H2(g)