题目内容
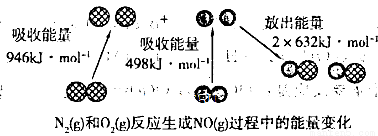
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如下图为N2(g)与 O2(g)反应生成NO(g)过程中的能量变化:
下列说法正确的是
A.1 mol N2(g)和1 molO2 (g)具有的总能量大于 2 mol NO(g)具有的总能量
B.1 molN2 (g)和l molO2 (g)反应生成2 mol NO(g)吸收180 kJ热量.
C.通常情况下N2(g)和O2(g)混合能直接反应生成NO
D.数据不足,不能确定反应热的大小
B
【解析】
试题分析:分析题给示意图,依据反应焓变=反应物断裂化学键吸收的能量-生成物形成化学键放出的能量计算:该反应的焓变为△H=946kJ/mol+498kJ/mol-2×632kJ/mol=+180kJ/mol,为吸热反应。A、该反应为吸热反应,1 mol N2(g)和1 molO2 (g)具有的总能量小于 2 mol NO(g)具有的总能量,错误;B、1 molN2 (g)和l molO2 (g)反应生成2 mol NO(g)吸收180 kJ热量,正确;C、通常情况下N2(g)和O2(g)混合不能直接反应生成NO,二者反应需要放的条件,错误;D、题给数据能确定反应热的大小,错误。
考点:考查化学反应与能量变化、化学反应的焓变计算及氮气的化学性质。

练习册系列答案
 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目