题目内容
质量相同的两种气体A、B,在同温同压下,A的密度大于B.下列说法错误的是( )
| A、相同条件下A占的体积比B大 |
| B、A的摩尔质量比B大 |
| C、A的分子数比B少 |
| D、A的物质的量比B小 |
考点:阿伏加德罗定律及推论
专题:阿伏加德罗常数和阿伏加德罗定律
分析:同温同压下,气体摩尔体积相等,根据ρ=
知,其密度之比等于摩尔质量之比,A的密度大于B,则A的摩尔质量大于B,相同质量的A、B,A的物质的量小于B,再结合V=nVm、N=nNA进行计算解答.
| M |
| Vm |
解答:
解:同温同压下,气体摩尔体积相等,
A.根据V=
知,相同质量时,体积与密度成反比,二者质量相等、A的密度大于B,所以A的体积小于B,故A错误;
B.根据ρ=
知,其密度之比等于摩尔质量之比,A的密度大于B,则A的摩尔质量大于B,故B正确;
C.A的摩尔质量大于B,相同质量的A、B,A的物质的量小于B,根据N=nNA知,其分子数与物质的量成正比,所以A的分子数小于B,故C正确;
D.A的摩尔质量大于B,相同质量的A、B,A的物质的量小于B,故D正确;
故选A.
A.根据V=
| m |
| ρ |
B.根据ρ=
| M |
| Vm |
C.A的摩尔质量大于B,相同质量的A、B,A的物质的量小于B,根据N=nNA知,其分子数与物质的量成正比,所以A的分子数小于B,故C正确;
D.A的摩尔质量大于B,相同质量的A、B,A的物质的量小于B,故D正确;
故选A.
点评:本题考查阿伏伽德罗定律及其应用,明确物质的量公式中各个物理量的关系是解本题关键,注意气体摩尔体积的适用范围及适用条件,题目难度不大.

练习册系列答案
相关题目
工业上制取硫酸,回收尾气中的废气常选用的试剂是( )
| A、氨水 |
| B、NaOH |
| C、H2SO4 |
| D、H2SO3 |
A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大.已知:B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物对应的水化物与其氢化物反应能生成盐,D与E同主族,E元素原子的最外层电子数比次外层电子数少2.由元素A、B、D组成的一元酸X为日常生活中的调味剂,元素A、F组成的化合物为Y,A与C形成的气态化合物Z在标准状况下的密度为0.76g/L,Z溶于水所得溶液为W.下列说法正确的是( )
| A、元素C在周期表中的位置是第三周期第ⅤA族 |
| B、在等体积、等pH的X、Y溶液中分别加入等质量的锌粉,充分反应后仅有一份溶液中存在锌粉,则反应过程中两溶液中反应速率的大小关系是:X<Y |
| C、由A、B、C、D四种元素形成的化合物一定只有共价键 |
| D、25℃时,将W溶液与Y溶液等体积混合,充分反应后若pH=7则c(W)>c(Y) |
下列说法正确的是( )
| A、4.2 g丙烯中所含的共价键数目为0.6×6.02×1023 |
| B、含1 mol H2SO4的浓硫酸与足量铜反应转移的电子总数为6.02×1023 |
| C、相同条件下,1 L CO和H2的混合气体完全燃烧消耗0.5 L O2 |
| D、相同物质的量的OH-和CH3+含有相同数目的电子 |
NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A、5.6 g 铁在足量氯气中燃烧,电子转移0.2 NA |
| B、标准状况下,2.24 L水中含有水分子0.1 NA |
| C、1.12 L氯气中含有氯原子0.1 NA |
| D、32克O2所含的氧原子数目为2NA |
同温同压下两个容积相等的贮气瓶,一个装有NO气体,另一个装有O2和N2的混合气体,则两瓶内的气体不一定相同的是( )
| A、气体质量 | B、气体的物质的量 |
| C、分子总数 | D、原子数 |
火星表面还有火星表面还有黄钾铁矾,其组成的化学式为KFe3(SO4)2(OH)6,易溶于稀硫酸,下列说法不正确的是( )
| A、黄钾铁矾中铁元素显+3价 |
| B、黄钾铁矾属于碱 |
| C、黄钾铁矾溶于硫酸后,滴加KSCN溶液,溶液变红 |
| D、黄钾铁矾晶体在酒精灯火焰上灼烧,透过蓝色的钴玻璃可观察到紫色火焰 |
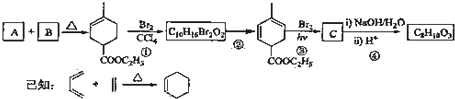
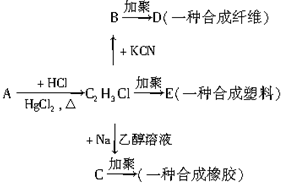 卤代烃里的卤原子易与活泼金属阳离子结合,发生下列反应:
卤代烃里的卤原子易与活泼金属阳离子结合,发生下列反应: