题目内容
下列说法或表示方法正确的是( )
| A、已知H2(g)+I2(g)?2HI(g)△H=-9.48 kJ?mol-1,则在一定条件下将1 mol H2(g)和1 mol I2(g)置于一密闭容器中充分反应后,最多可放出9.48 kJ的热量 |
| B、由C(石墨)→C(金刚石);△H=+119kJ?mol-1可知,金刚石比石墨稳定 |
| C、在稀溶液中:H+(aq)+OH-(aq)═H2O(l);△H=-57.3kJ?mol-1,若将含0.5mol H2SO4的浓硫酸与含1mol NaOH的稀溶液混合,放出的热量大于57.3kJ |
| D、在101kPa、25℃时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=-285.8kJ?mol-1 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、可逆反应的反应物不能完全转化;
B、根据物质的总能量与稳定性关系判断;
C、浓硫酸溶于水放热;
D、注意化学计量数与反应热对应.
B、根据物质的总能量与稳定性关系判断;
C、浓硫酸溶于水放热;
D、注意化学计量数与反应热对应.
解答:
解:A、上述为可逆反应,可能反应的反应物不能完全转化,故A错误;
B、石墨转化为金刚石吸热,说明石墨的总能量小于金刚石的总能量,石墨比金刚石稳定,故B错误;
C、浓硫酸溶解时放热,所以将含0.5mol H2SO4的浓硫酸与含1mol NaOH的稀溶液混合,放出的热量大于57.3kJ,故C正确;
D、2g氢气是1mol,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ?mol-1,故D错误.
故选C.
B、石墨转化为金刚石吸热,说明石墨的总能量小于金刚石的总能量,石墨比金刚石稳定,故B错误;
C、浓硫酸溶解时放热,所以将含0.5mol H2SO4的浓硫酸与含1mol NaOH的稀溶液混合,放出的热量大于57.3kJ,故C正确;
D、2g氢气是1mol,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ?mol-1,故D错误.
故选C.
点评:本题考查化学反应能量,题目难度不大,注意理解反应热与能量的关系,能量与稳定性的关系.

练习册系列答案
相关题目
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用.已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiOOH+2H2O
Cd(OH)2+2Ni(OH)2,下列说法不正确的是( )
| 放电 |
| 充电 |
| A、放电时化学能不能全部转化为电能 |
| B、放电时Cd为该电池的负极,充电时这一端应接直流电源的正极 |
| C、放电时该电池的正极反应为:NiOOH+H2O+e-═Ni(OH)2+OH- |
| D、充电时,阴极反应为:Cd(OH)2+2e-═Cd+2OH- |
有4种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成:①NH4Cl与NaOH;②NH4Cl与HCl; ③NH4Cl与NaCl; ④NH4Cl与AlCl3;下列各项排序正确的是( )
| A、pH:②>③>④>① |
| B、c(NH4+):②>④>③>① |
| C、c(Cl-):①>③>②>④ |
| D、c(NH3?H2O):①>④>③>② |
将a g镁加入一定量的稀硫酸,使恰好完全溶解,得到b L气体,所得溶液中共有c个溶质的离子.阿伏加德罗常数为NA,则下列关系式正确的是( )
A、NA=
| ||||
B、NA=
| ||||
C、
| ||||
| D、以上均不一定正确 |
下列有关金属键的叙述错误的是( )
| A、金属键没有饱和性,没有方向性 |
| B、金属键是金属阳离子和自由电子间的强烈的静电吸引作用 |
| C、金属键中的自由电子属于整块金属 |
| D、金属的物理性质和金属固体的形成都与金属键有关 |
在加入铝能放出气体的某无色溶液中,下列离子可以大量共存的是( )
| A、NH4+、Mg2+、Ba2+、HCO3-、Cl- |
| B、Na+、Cu2+、Ca2+、SO42-、NO3- |
| C、Ba2+、Mg2+、NH4+、SO42-、Cl- |
| D、K+、Na+、Cl-、CO32-、NO3- |
下列说法错误的是( )
| A、需要加热才能发生的反应一定是吸热反应 |
| B、在热化学方程式中无论反应物还是生成物均必须标明聚集状态 |
| C、焓变小于0而熵变大于0的反应肯定是自发的 |
| D、轮船水线以下的船体上嵌入一定量的锌块可减缓海水对轮船的腐蚀 |
常温下,已知0.1mol?L-1的CH3COOH和HCN溶液的PH分别为a、b,且1<a<b.下列有关叙述不正确的是( )

| A、常温下,等浓度的CH3COONa溶液和NaCN溶液的PH前者较小 |
| B、在NaCN溶液中:c (Na+)+c (H+)═c (OH-)+c (CN-) |
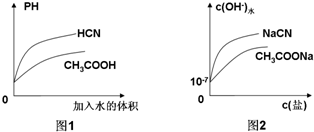
| C、相同温度下,相同PH的CH3COOH和HCN溶液分别加水稀释,溶液PH随溶液体积变化的曲线如图1所示 |
| D、常温下,CH3COONa溶液和NaCN溶液中由水电离出的c(OH-)与盐浓度的变化曲线如图2所示 |
N-H键键能为391.5kJ/mol,其含义是( )
| A、由N和H形成1 mol NH3所放出的能量 |
| B、把1 mol NH3中的共价键全部拆开所吸收的能量 |
| C、拆开NA个N-H键所吸收的能量 |
| D、形成1个 N-H键所放出的能量 |