题目内容
【题目】下列说法正确的是( )
A.任何情况下,温度都不可能对反应的方向起决定性作用
B.室温下,CH3COOH的KW=1.7×10﹣5 , NH3H2O的Kb=1.7×10﹣5 , CH3COOH溶液中的c(H+)与NH3H2O中的c(OH﹣)相等
C.用pH试纸测定溶液pH的正确操作是,将一小条试纸在待测液中蘸一下,取出后放在表面皿上,与标准比色卡对照
D.pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍
【答案】D
【解析】解:A、如△H>0,△S>0,高温下反应能自发进行,低温下不能自发进行,温度可能对反应的方向起决定性作用,故A错误;
B、室温下,醋酸溶液中c(H+)= ![]() ,氨水溶液中c(OH﹣)=
,氨水溶液中c(OH﹣)= ![]() ,两种溶液的浓度相对大小未知,所以无法判断醋酸溶液中氢离子浓度和氨水中氢氧根离子浓度的相对大小,故B错误;
,两种溶液的浓度相对大小未知,所以无法判断醋酸溶液中氢离子浓度和氨水中氢氧根离子浓度的相对大小,故B错误;
C、一试纸不能直接插入液面以下,应用玻璃棒蘸取或用滴管滴加,防止污染药品,故C错误;
D、pH=4.5的番茄汁中c(H+)=10﹣4.5 , pH=6.5的牛奶中c(H+)=10﹣6.5 , ![]() =100,故D正确;
=100,故D正确;
故选D.
【考点精析】利用弱电解质在水溶液中的电离平衡对题目进行判断即可得到答案,需要熟知当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理.

【题目】某溶液中可能含有的离子如下表所示:
可能大量含有的阳离子 | H+、Mg2+、Al3+、NH4+、Fe3+ |
可能大量含有的阴离子 | Cl-、NO3-、SO42-、CO32-、AlO2- |
为探究其成分,进行了探究实验。取一定量的溶液,向其中逐滴加入氢氧化钠溶液,产生沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)的关系如图所示:

(1)该溶液中一定不存在的阳离子是_____________
(2)该溶液中一定不存在的阴离子是_____________
(3)该溶液中含有的阳离子其对应的物质的量浓度之比为____________________________
(4)写出沉淀减少过程中发生反应的离子方程式____________________________
【题目】SO2的烟气会形成酸雨,危害环境.利用钠碱循环法可脱除烟气中的SO2 . 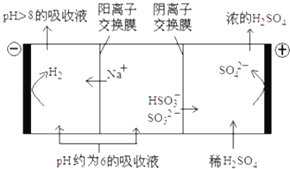
(1)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是 .
(2)吸收液吸收SO2的过程中,pH随n(SO32﹣),n(HSO3﹣)变化关系如下表:
n(SO32﹣):,n(HSO3﹣) | 91:9 | 1:1 | 1:91 |
PH | 8.2 | 7.2 | 6.2 |
1表判断NaHSO3溶液显性,用化学平衡原理解释:
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):
a.c(Na﹣)=2c(SO ![]() )+c(HSO
)+c(HSO ![]() )
)
b.c(Na﹣)>c(HSO ![]() )>c(SO
)>c(SO ![]() )>c(H﹣)=c(OH﹣)
)>c(H﹣)=c(OH﹣)
c.c(Na+)+c(H+)=c(SO ![]() )+c(HSO
)+c(HSO ![]() )+c(OH﹣)
)+c(OH﹣)
(3)当吸收液的pH降至约为6时,送至电解槽再生.再生示意图如下:
①HSO3﹣在阳极放电的电极反应式是 .
②当阴极室中溶液PH升至8以上时,吸收液再生并循环利用.简述再生原理: .
【题目】回答下列问题
肼是一种高能燃料.已经各共价键键能(断裂或形成1mol共价键时吸收或释放的能量)如下:
N≡N | O=O | N﹣N | N﹣H | O﹣H | |
键能(KJmol﹣1) | 946 | 497 | 154 | 391 | 463 |
(1)N2H4(g)+O2(g)N2(g)+2H2O(l)△H=KJmol﹣1
(2)Ⅱ.密闭容器中进行反应:3Fe(s)+4H2O(g)Fe3O4(s)+4H2(g)△H<02反应的化学平衡表达式为K= .
(3)已知:600℃时,上述反应的平衡常数K=16.现有如图1甲(恒温恒压)和如图1乙(恒温恒容)两容器,起始时按下表所示分别加入各物质,体积为2L,在600℃时反应经过一段时间后均达平衡.
Fe | H2O(g) | Fe3O4 | H2 | |
甲/mol | 2.0 | 1.0 | 2.0 | 0.5 |
乙/mol | 2.0 | 2.0 | 2.0 | 1.0 |
①关于甲、乙容器,下列说法正确的是
A.反应开始时两容器内的逆反应速率:甲<乙
B.若甲容器内气体的密度不再变化,则说明反应已达到平衡状态
C.若乙容器内气体的压强不再变化,则说明反应已达到平衡状态
D.平衡后添加Fe3O4 , 两容器内的平衡均逆向移动
②投料后甲5min达平衡,则此段时间内的平均反应速率v(H2)=
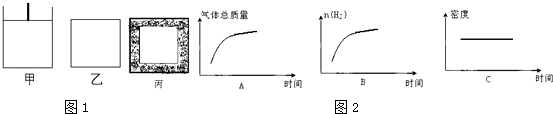
③平衡后若将乙容器体系温度突然降低100℃,如图2下述图象中能正确反映平衡移动过程中容器内变化情况的是 .
(4)为恒容绝热容器,进行上述反应,起始与平衡时的各物质的量见下表:
Fe | H2O(g) | Fe3O4 | H2 | |
起始/mol | 3.0 | 3.0 | 0 | 0 |
平衡/mol | m | n | p | q |
若在达到平衡后的容器丙中,分别按照下列A、B、C三种情况继续添加各物质,则再次达平衡时,容器丙中H2的百分含量按由大到小的顺序(用A、B、C表示).
Fe | H2O(g) | Fe3O4 | H2 | |
A/mol | 3.0 | 3.0 | 0 | 0 |
B/mol | 0 | 0 | 3.0 | 3.0 |
C/mol | m | n | p | q |
25℃时,Fe(OH)3的ksp=4ⅹ10﹣38 , 现有盐酸酸化的0.08mol/L的FeCl3溶液,其PH=1,向其中加入等体积的mol/L的NaOH溶液,可恰好开始析出沉淀(混合时溶液体积可直接加和).