题目内容
【题目】某研究性学习小组同学用含有少量泥沙、CaCl2、MgCl2、Na2SO4的粗盐制取纯净的NaCl,实验前他们设计了如图方案(框图)
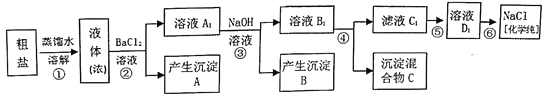
(1)请写出操作第④步所加试剂名称及第②步操作名称:
④_____________________,②___________________________。
(2)写出第⑤步操作中可能发生反应的离子方程式:____________________。
(3)如何检验第②步操作中硫酸根离子已完全除尽:_____________________。
(4)你认为该设计里哪些步骤调换后不影响实验结果:___________________。
【答案】碳酸钠 过滤 CO32-+2H+=H2O+CO2↑;H++OH-=H2O 取A1中溶液少许,滴加氯化钡溶液,若无浑浊产生,则硫酸根离子已完全除尽 ②与③或③与④
【解析】
(1)根据操作第④、⑤步所加试剂名称及第⑥步操作的原理分析,碳酸钠会除去反应剩余的氯化钡,离子都形成沉淀,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,最后经蒸发操作得到较纯净的氯化钠;
(2)溶液中含有过量的氢氧化钠、碳酸钠以及要保留的氯化钠溶液,可以再加入盐酸将碳酸钠和氢氧化钠除掉;
(3)根据SO42-+Ba2+=BaSO4↓,产生白色沉淀进行解答;
(4)先除镁离子,还是先除硫酸根离子都行,但是加入的碳酸钠要放在加入的氯化钡之后;
(1)操作第④步是除Ca2+,加Na2CO3溶液转化为沉淀,Ca2++CO32-=CaCO3↓,同时碳酸钠还除去反应剩余的氯化钡溶液引入的杂质Ba2+,Ba2++CO32-=BaCO3↓;
操作②是分离难溶性固体与溶液混合物的方法,名称是过滤;
(2)滤液C1中含有过量的氢氧化钠、碳酸钠及要保留的氯化钠溶液,可向该溶液中加入足量的盐酸,盐酸与杂质碳酸钠和氢氧化钠反应变为气体或水除掉,反应的离子方程式是:H++OH-=H2O ;CO32-+2H+=H2O+CO2↑ ;
(3)向混合溶液中加入BaCl2溶液,发生反应:SO42-+Ba2+=BaSO4↓,产生白色硫酸钡沉淀,若硫酸根离子已完全除尽,那么取A1中溶液少许,滴加氯化钡溶液,就不会出现浑浊现象;若出现浑浊现象,证明溶液中还存在硫酸根离子;
(4)首先要把粗盐溶于水形成溶液,然后Mg2+用OH-沉淀除去,加入过量的氢氧化钠可以将镁离子沉淀,SO42-用Ba2+沉淀,加入过量的氯化钡可以将Ba2+沉淀,至于先除Mg2+,还是先除SO42-都没有关系,Ca2+用CO32-沉淀,除Ca2+加入碳酸钠转化为沉淀,Ca2++CO32-=CaCO3↓,但是加入的碳酸钠一定要放在加入的氯化钡之后,这样碳酸钠溶液既可以除去原溶液中的CaCl2,也可以除去因除Na2SO4杂质加入的过量的BaCl2溶液,Ba2++CO32-=BaCO3↓,离子都形成沉淀,一起进行过滤,所以②与③或③与④步骤调换顺序,不影响实验结果;

【题目】某实验小组同学做中和滴定和中和热的测定两个实验。
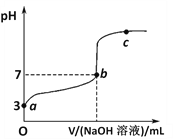
Ⅰ.下图是该小组同学用0.5000 mol/L的盐酸滴定某未知浓度的NaOH溶液的示意图和第1次滴定前、后盛放盐酸的滴定管中液面的位置。请回答下列问题。

(1)仪器A的名称是_______________。
(2)第1次滴定消耗标准液_________mL 。
(3)已知每次滴定操作所取待测NaOH溶液的体积均为20.00mL。第2、3、4次滴定数据如下表所示。通过计算得待测NaOH溶液的平均浓度是___________mol/L。(保留四位有效数字)
实验 编号 | 待测NaOH溶液的体积(mL) | 滴定前盐酸的 体积读数(mL) | 滴定后盐酸的 体积读数(mL) |
2 | 20.00 | 1.20 | 21.20 |
3 | 20.00 | 2.24 | 22.26 |
4 | 20.00 | 1.50 | 21.48 |
(4)滴定操作可分解为如下几步(所用的仪器刚用蒸馏水洗净):
A.向锥形瓶里注入20.00 mL待测NaOH溶液,并滴入2-3滴酚酞;
B.用标准溶液润洗酸式滴定管2-3次;
C.固定好装标准溶液的酸式滴定管,调节滴定管尖嘴使之充满溶液,管内无气泡;
D.取标准HCl溶液注入酸式滴定管至刻度0以上2-3cm;
E.调节液面至0或0以下刻度,记下读数;
F.把锥形瓶放在滴定管下面,用标准HCl溶液滴定至终点并记下滴定管液面刻度。
合理的操作顺序是(用序号字母填写)______________________________。
(5)如何判断到达滴定终点?_________________________________________。
(6)如果上述B步骤省略,对测定结果的影响是_________;标准液读数时,若滴定前仰视,滴定后俯视,对测定结果的影响是______(填“无影响”、“偏高”、“偏低”)。
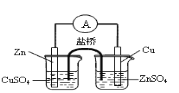
Ⅱ.现用上述盐酸和已测出浓度的NaOH溶液,设计如下装置测定中和热。
将50mL盐酸与50mL NaOH溶液在图示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(7)从图示看此装置存在错误,请指出_________________。
(8)当室内温度低于10℃时,对实验数据影响很大,实验测得的中和热数值偏小。其原因是___________________。
(9)如果实验测得起始温度为t1℃,反应后的最高温度为t2℃,则中和热的表达式为ΔH =___________。(中和后溶液的比热容c=4.18J/(g.℃))
(10)本次实验室内温度正常,操作无误,但是数据偏低,其原因是_________________。
【题目】下表是某城市某日空气质量报告:
污染指数 | 首要污染物 | 空气质量级别 | 空气质量状况 |
55 | SO2 | II | 良 |
该市某校研究性学习小组对表中首要污染物SO2导致酸雨的成因进行探究。
实验一:用下图所示装置进行实验。
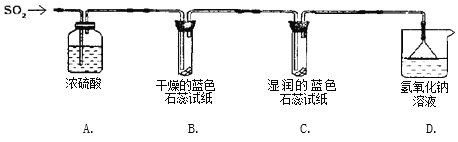
(1)A装置的作用是______________。
(2)实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊试纸变成_____色,说明SO2与水反应生成一种酸。
(3)D装置的作用是_________ ,写出反应的化学方程式_____________________________。
实验二:往盛有水的烧杯中通入SO2气体,测得所得溶液的pH_______7(填“>”“=”或“<”),然后每隔1 h测定其pH,发现pH逐渐变小,直至恒定。说明烧杯中溶液被空气中的氧气氧化最终成_______。
(查阅资料) SO2形成酸雨的另一途径:SO2与空气中的O2在飘尘的作用下反应生成SO3,SO3溶于降水生成H2SO4。在此过程中飘尘作_____。
(探究结论)SO2与空气中的氧气、水反应生成硫酸而形成酸雨。该市可能易出现酸雨。
(1)酸雨造成的危害是:______________________________。
(2)汽车排放的尾气,硝酸、化肥等工业生产排出的废气中都含有氮的氧化物,氮的氧化物溶于水最终转化为____________,是造成酸雨的另一主要原因。
(提出建议)该市汽车数量剧增,为了减少汽车尾气造成的污染,建议市政府推广使用混合型汽油,即往汽油中按一定比例加人_________(填“水”或“乙醇”)。