题目内容
【题目】下列关于各实验装置图的叙述中正确的是
A. 构成锌铜原电池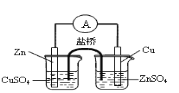
B. 实验室制氨气并收集干燥氨气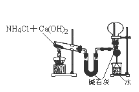
C. 验证溴乙烷发生消去反应生成烯烃
D. 由实验现象推知酸性强弱顺序为CH3COOH>H2CO3>苯酚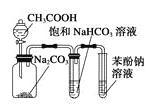
【答案】BD
【解析】
A项,应将锌插入硫酸锌,铜插入硫酸铜溶液中;B项,收集干燥氨气,在用水吸收氨气前面、收集装置后面连接盛有碱石灰的干燥管;C项,应在两装置中间加一个除去乙醇蒸气的装置,错误;CH3COOH酸性强于H2CO3、H2CO3强于苯酚,要用饱和碳酸氢钠溶液除去乙酸,排除乙酸的干扰。
A.应将锌插入硫酸锌,铜插入硫酸铜溶液中,否则锌置换铜,能形成原电池反应,但不能形成电流,错误;B.收集氨气后面连接盛有碱石灰的干燥管,可以防止用水吸收氨气的装置中水蒸气进入收集的氨气中,得到干燥的氨气,正确;C.乙醇易挥发,其能与酸性高锰酸钾溶液反应,应先除去乙醇,错误;D.乙酸和碳酸钠溶液反应生成二氧化碳气体,用饱和碳酸氢钠除去挥发的醋酸,二氧化碳气体通入到苯酚钠溶液,溶液变浑浊,可说明酸性CH3COOH>H2CO3>C6H5OH,正确。
故选BD。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】向2L密闭容器中加入1molNO和1mol活性炭,发生反应:2NO(g)+C(s) ![]() N2(g)+CO2(g) △H = -213.5kJ/mol,达到平衡的数据如下:
N2(g)+CO2(g) △H = -213.5kJ/mol,达到平衡的数据如下:
温度/℃ | n(活性炭)/mol | n(CO2)/mol |
T1 | 0.70 | —— |
T2 | —— | 0.25 |
下列说法不正确的是( )
A. 上述信息可推知:T1<T2
B. T1℃时,该反应的平衡常数K=9/16
C. T1℃时,若开始时反应物的用量均减小一半,平衡后NO的转化率减小
D. T2℃时,若反应达平衡后再缩小容器的体积。c(N2)/c(NO)不变