题目内容
18.钠在坩埚中燃烧不可以证明的是( )| A. | 钠的熔、沸点低 | |
| B. | 钠的颜色是银白色的 | |
| C. | 钠与空气中氧气反应,条件不同产物不同 | |
| D. | 因为反应要加热,所以该反应是吸热反应 |
分析 A.Na的熔点较低加热熔化;
B.钠的颜色是银白色的;
C.Na在空气中氧化成氧化钠,燃烧生成过氧化钠;
D.需加热的反应不一定为吸热反应.
解答 解:A.Na的熔点较低,受热是先熔化,然后燃烧,故A不选;
B.切取一小块钠,切口处可观察到钠的颜色是银白色的,故B不选;
C.钠在没有条件下和氧气反应生成氧化钠,在点燃条件下,和氧气反应生成淡黄色的过氧化钠,故C不选;
D.钠在坩埚中加热,先熔化,然后燃烧,所以该反应是放热反应,故D选;
故选D.
点评 本题考查了Na的化学性质,主要涉及了钠与氧气的反应,钠的颜色和熔、沸点以及与氧气反应的热效应,题目难度不大.

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
2.根据如图海水综合利用的工业流程图,判断下列说法正确的是.( )
已知:MgCl2.6H2O受热生成Mg(OH) Cl和HC1气体等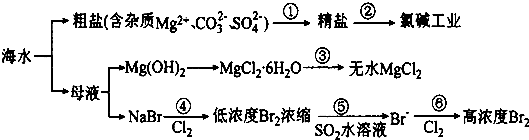
已知:MgCl2.6H2O受热生成Mg(OH) Cl和HC1气体等

| A. | 过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质 | |
| B. | 过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题 | |
| C. | 在过程④、⑥反应中每氧化0.2 mol Br一需消耗2.24LCl2 | |
| D. | 在过程③中将MgCl2.6H2O灼烧即可制得无水MgCl2 |
13.已知:酸性H2CO3>HClO>HCO${\;}_{3}^{-}$,判断在等浓度的NaClO、NaHCO3混合溶液中,各种离子浓度关系正确的是( )
| A. | c(Na+)>c(HCO${\;}_{3}^{-}$)>c(H+)>c(OH-) | |
| B. | c(HCO${\;}_{3}^{-}$)>c(ClO-)>c(OH-) | |
| C. | c(HClO)+c(ClO-)=c(HCO${\;}_{3}^{-}$)+c(H2CO3) | |
| D. | c(Na+)+c(H+)=c(HCO${\;}_{3}^{-}$)+c(ClO-)+c(OH-)+c(CO${\;}_{3}^{2-}$) |
3.下列说法正确的是( )
| A. | 酿酒过程中,葡萄糖可通过水解反应生成酒精 | |
| B. | 工业上利用油脂生产肥皂、用淀粉酿酒、用纤维素生产酒精 | |
| C. | 酸性高锰酸钾紫色溶液中加入植物油充分振荡后,溶液颜色不会因反应褪去 | |
| D. | 蛋白质和油脂在发生腐败变质时,均会产生含NH3的刺激性气味 |
10.实验室中某溶液含有Ag+、Cu2+、Ba2+,若依次加入试剂使三种离子分别沉淀出来,过滤得到相应的沉淀,则加入试剂的顺序为( )
| A. | NaOH、Na2SO4、NaCl | B. | NaCl、Na2SO4、NaOH | ||
| C. | NaOH、NaCl、Na2SO4 | D. | Na2SO4、NaOH、NaCl |
8.乙醇是重要的有机化工原料,可由乙烯直接水合法或间接水合法生产.回答下列问题:
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯(C2H5OSO3H).再水解生成乙醇.写出相应的反应的化学方程式C2H4+H2SO4=C2H5OSO3H、C2H5OSO3H+H2O→C2H5OH+H2SO4.
(2)已知:乙烯气相直接水合反应如下:
C2H4(g)+H2O(g)?C2H5OH(g) H=-45.5KJ/mol
下图为气相直接水合法中乙烯的平衡转化率与温度、压强的关系(其中n(H2O):n(C2H4)=1:1)

①计算乙烯水合制乙醇反应在图中A点的平衡常数Kp=0.07(MPa)-1(Kp表示用平衡分压代替平衡浓度计算出的平衡常数的值,分压=总压×物质的量分数)
②图中压强P1、P2、P3、P4的大小顺序为:p1<p2<p3<p4,理由是反应分子数减少,相同温度下,压强升高乙烯转化率提高.
(3)若某温度下,反应C2H4(g)+H2O(g)?C2H5OH(g)的平衡常数为Kp=0.05MPa-1,体系总压为8.00MPa,各物质的量分数如下表所示.
则v(正)<v(逆)(填“>”“<”“=”).
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯(C2H5OSO3H).再水解生成乙醇.写出相应的反应的化学方程式C2H4+H2SO4=C2H5OSO3H、C2H5OSO3H+H2O→C2H5OH+H2SO4.
(2)已知:乙烯气相直接水合反应如下:
C2H4(g)+H2O(g)?C2H5OH(g) H=-45.5KJ/mol
下图为气相直接水合法中乙烯的平衡转化率与温度、压强的关系(其中n(H2O):n(C2H4)=1:1)

①计算乙烯水合制乙醇反应在图中A点的平衡常数Kp=0.07(MPa)-1(Kp表示用平衡分压代替平衡浓度计算出的平衡常数的值,分压=总压×物质的量分数)
②图中压强P1、P2、P3、P4的大小顺序为:p1<p2<p3<p4,理由是反应分子数减少,相同温度下,压强升高乙烯转化率提高.
(3)若某温度下,反应C2H4(g)+H2O(g)?C2H5OH(g)的平衡常数为Kp=0.05MPa-1,体系总压为8.00MPa,各物质的量分数如下表所示.
| 物质 | C2H4(g) | H2O(g) | C2H5OH(g) |
| 物质的量分数 | 0.25 | 0.25 | 0.5 |