题目内容
4.实验中加热KClO3和MnO2的混合物制取O2,若要收集448mL(STP)O2,发生反应的KClO3的质量是多少?分析 n(O2)=$\frac{0.448L}{22.4L/mol}$=0.02mol,根据2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑发生反应的KClO3的物质的量,带入m=n•M计算质量.
解答 解:收集448mL(STP)O2的物质的量n(O2)=$\frac{0.448L}{22.4L/mol}$=0.02mol,设发生反应的KClO3的物质的量为x,则
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
2 3
x 0.02mol
$\frac{x}{0.02mol}=\frac{2}{3}$,解得x=0.013mol,
KClO3的质量m=0.013mol×122.5g/mol=1.59g,
答:若要收集448mL(STP)O2,发生反应的KClO3的质量是1.59g.
点评 本题考查根据方程式进行的计算,比较基础,旨在考查学生对基础知识的理解掌握.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
15.下列对药物的认识和使用的说法,正确的是( )
| A. | 麻黄碱属于非处方药 | B. | 感冒时服用适量阿司匹林 | ||
| C. | 冰毒和海洛因不是毒品 | D. | 大部分药物都没有毒副作用 |
16.下列解释事实的方程式不正确的是( )
| A. | 用Na2S除去废水中的Hg2+:Hg2++S2-═HgS↓ | |
| B. | Na在氧气中燃烧产生淡黄色固体:2Na+O2$\frac{\underline{\;\;△\;\;}}{\;}$Na2O2 | |
| C. | 将NO2通入水中,生成硝酸:3NO2+H2O═2H++2NO3-+NO | |
| D. | Al与NaOH水溶液反应产生气体:Al+OH-+2H2O═Al(OH)3↓+2H2↑ |
20.关天单键、双键、叁键的说法正确的是( )
| A. | 单键的键长最短,键能最大 | |
| B. | 叁键的键长最短,键能最大 | |
| C. | 双键中两个键都活泼,加成时都断裂 | |
| D. | 只有碳原子间才能形成双键和叁键 |
 bB(g)+cC(g),在温度不变的条件下,再充入一定量的A,重新达到平衡时,下列判断中正确的是( )
bB(g)+cC(g),在温度不变的条件下,再充入一定量的A,重新达到平衡时,下列判断中正确的是( )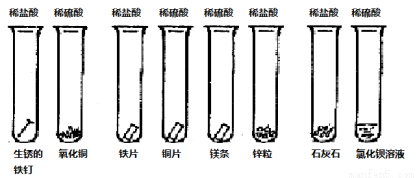
 。
。