题目内容
14.下列反应中水的作用与其他三个反应明显不同的是( )| A. | Cl2和H2O | B. | NO2和H2O | C. | Na和H2O | D. | Na2O2和H2O |
分析 根据反应前后水中各元素化合价的变化确定水的作用,元素的化合价升高的作还原剂,化合价降低的作氧化剂,以此解答该题.
解答 解:A.反应Cl2+H2O=HCl+HClO中,水中各元素的化合价不变,所以水既不是氧化剂又不是还原剂;
B.反应3NO2+H2O=2HNO3+NO中,水中各元素的化合价不变,所以水既不是氧化剂又不是还原剂;
C.反应2Na+2H2O=2NaOH+H2↑中,水中氢元素化合价降低,所以水作氧化剂;
D.反应2Na2O2+2H2O=4NaOH+O2↑中,水中各元素的化合价不变,所以水既不是氧化剂又不是还原剂.
则水的作用与其他三个反应明显不同的是C.
故选C.
点评 本题以水的作用为载体考查了氧化还原反应,为高频考点,侧重考查学生的分析能力,难度不大,根据元素化合价变化来判断物质的性质即可.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
9.有一系列有机物分子,每个碳原子与周围3个碳原子形成碳碳单键,碳原子剩余价键被氢原子饱和.其中甲、乙、丙三种有机物结构如图所示,下列关于它们的描述正确的是( )

| A. | 甲、乙、丙组成结构相似,互为同系物 | |
| B. | 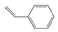 是丙的同分异构体 是丙的同分异构体 | |
| C. | 乙的二氯代物有4种 | |
| D. | 甲、乙、丙均为不饱和烃,它们都能使溴的CCl4溶液褪色 |
5.下列变化属于物理变化的是( )
| A. | 乙烯通入酸性高锰酸钾溶液褪色 | B. | 甲烷在空气中燃烧 | ||
| C. | 钠与酒精混合有气泡 | D. | 苯滴入溴水中振荡后水层接近无色 |
2.下列叙述正确的是( )
| A. | 元素的单质一定由氧化或还原该元素的化合物制得 | |
| B. | 一个氧化还原反应中,氧化剂和还原剂一定是两种不同的物质 | |
| C. | 阳离子只能得到电子被还原,阴离子只能失去电子被氧化 | |
| D. | 含有最高价元素的化合物不一定具有很强的氧化性 |
19.下列说法中,正确的是( )
| A. | SO2能使酸性KMnO4溶液褪色,说明SO2具有还原性 | |
| B. | SO2能使品红溶液褪色,其漂白原理与氯水相同 | |
| C. | SO2是酸性氧化物,可以用澄清石灰水来鉴别SO2与CO2 | |
| D. | 用水吸收硫在过量氧气中燃烧的产物,可用于工业制备硫酸 |
6. 如图所示,夹子开始处于关闭状态,将液体A96℃的水①空气(标准大气压)气体B②液体A夹子滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了.则液体A和气体B组合
如图所示,夹子开始处于关闭状态,将液体A96℃的水①空气(标准大气压)气体B②液体A夹子滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了.则液体A和气体B组合
不可能是下列的( )
 如图所示,夹子开始处于关闭状态,将液体A96℃的水①空气(标准大气压)气体B②液体A夹子滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了.则液体A和气体B组合
如图所示,夹子开始处于关闭状态,将液体A96℃的水①空气(标准大气压)气体B②液体A夹子滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了.则液体A和气体B组合不可能是下列的( )
| A. | NaOH溶液、CO2 | B. | H2O、NH3 | C. | NaOH溶液、NO | D. | H2O、NO2 |
3.18克葡萄糖(C6H12O6)与32克氧气充分反应生成二氧化碳和水蒸气,将生成的气体缓缓通过足量的过氧化钠固体,则固体增重( )克.
| A. | 18 | B. | 16 | C. | 32 | D. | 不能确定 |
